
下列各组物质性质比较中,正确的是( )
|
| A. | 氢化物沸点:HI>HBr>HCl>HF | B. | 离子半径:K+>Cl﹣>S2﹣ |
|
| C. | 分子稳定性:HF>HCl>HBr>HI | D. | 单质熔点:Li<Na<K<Rb |
考点:
元素周期律和元素周期表的综合应用.
专题:
元素周期律与元素周期表专题.
分析:
A.HF含有氢键,沸点最高;
B.核外电子排布相同的离子,核电核数越大半径越小;
C.元素的非金属性越强,对应的氢化物越稳定
D.碱金属元素的单质,原子序数越大,熔沸点越低.
解答:
解:A.HF含有氢键,沸点最高,HI、HCl、HBr不含氢键,相对分子质量越大,分子间作用力越强,沸点越高,则有氢化物沸点:HF>HI>HBr>HCl,故A错误;
B.K+、Cl﹣、S2﹣的核外电子排布相同的离子,核电核数越大半径越小,则有离子半径:K+<Cl﹣<S2﹣,故B错误;
C.非金属性:F>Cl>Br>I,元素的非金属性越强,对应的氢化物越稳定,则有HF>HCl>HBr>HI,故C正确;
D.碱金属元素的单质,原子序数越大,原子半径越大,熔沸点越低,则单质熔点:Li>Na>K>Rb,故D错误.
故选C.
点评:
本题考查元素周期表与元素周期律的综合应用,题目难度不大,本题注意把握元素周期律的递变规律,注重基础积累的积累即可.


 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
在一定条件下,将3molN2和3molH2充入一个容积固定的密闭容器中,发生反应N2(气)+3H2(气)⇌2NH3(气).当反应达到平衡时NH3为nmol.在与上述完全相同的容器中,保持温度不变,若平衡时NH3仍为n mol,则下列组合中不正确的是( )
| 起始状态/mol |
| ||
| N2 | H2 | NH3 | |
| A | 2 | 0 | 2 |
| B | 2.5 | 1.5 | 1 |
| C | 2 | ||
| D | 0 | 0 | 2 |
|
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知热化学方程式:SO2(g)+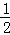 O2(g)⇌SO3(g)△H=﹣98.32kJ•mol﹣1,在容器中充入2mol SO2和1mol O2充分反应,最终放出的热量为( )
O2(g)⇌SO3(g)△H=﹣98.32kJ•mol﹣1,在容器中充入2mol SO2和1mol O2充分反应,最终放出的热量为( )
A. 196.64 kJ B. 98.32 kJ C. <196.64 kJ D. >196.64 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
“纳米材料”是粒子直径为1~100nm(纳米)的材料,纳米碳就是其中的一种.若将纳米碳均匀地分散到蒸馏水中,所形成的物质( )
①是溶液
②是胶体
③能产生丁达尔效应
④能透过滤纸
⑤不能透过滤纸
⑥静置后,会析出黑色沉淀.
|
| A. | ①④⑥ | B. | ②③⑤ | C. | ②③④ | D. | ①③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列与化学概念有关的说法正确的是( )
|
| A. | 化合反应均为氧化还原反应 |
|
| B. | 金属氧化物均为碱性氧化物 |
|
| C. | 催化剂能改变可逆反应达到平衡的时间 |
|
| D. | 石油是混合物,其分馏产品汽油为纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O反应中, 是氧化剂; 是还原剂; 元素被氧化; 元素被还原; 是氧化产物; 是还原产物.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.元素处于最高价态,一定具有最强的氧化性
B.阳离子只有氧化性,阴离子只有还原性
C.还原剂失电子越多,还原性越强
D.在化学反应中,某元素由化合态变为游离态,此元素可能被氧化,也可能被还原
查看答案和解析>>
科目:高中化学 来源: 题型:
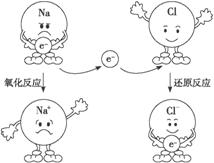
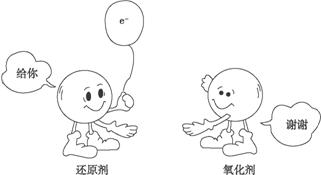
下图是以氯化钠为例表示的氧化反应、还原反应,以及氧化还原反应实质的示意图。认真分析示意图,总结归纳:什么是氧化反应?什么是还原反应 氧化还原反应的实质是什么?
______________________________________________________________________
______________________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
白蚁能分泌一种叫做蚁酸的物质,其化学性质与乙酸相似.据此推断,下列最不容易被蚁酸腐蚀的是( )
A. 黄金饰品 B. 镀锌水管 C. 铝合金门窗 D. 石灰墙面
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com