
 ¶ĢÖÜĘŚÖ÷×åŌŖĖŲA”¢B”¢C”¢DµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬CŗĶDĪ»ÓŚĶ¬Ņ»Ö÷×壮m”¢n”¢p¾łĪŖÓÉÕāŠ©ŌŖĖŲ×é³ÉµÄ¶žŌŖ»ÆŗĻĪļ£¬¼×”¢ŅŅ”¢±ūĪŖĘäÖŠČżÖÖŌŖĖŲ¶ŌÓ¦µÄµ„ÖŹ£¬±ūĪŖµ»ĘÉ«¹ĢĢ壬Ņ×ČÜŌŚBD2ÖŠ£¬pµÄĖ®ČÜŅŗŹĒŅ»ÖÖ¶žŌŖČõĖį£¬ÓŠĘư׊Ō£®ÉĻŹöĪļÖŹµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£Ø·“Ó¦Ģõ¼žŹ”ĀŌ£©£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
¶ĢÖÜĘŚÖ÷×åŌŖĖŲA”¢B”¢C”¢DµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬CŗĶDĪ»ÓŚĶ¬Ņ»Ö÷×壮m”¢n”¢p¾łĪŖÓÉÕāŠ©ŌŖĖŲ×é³ÉµÄ¶žŌŖ»ÆŗĻĪļ£¬¼×”¢ŅŅ”¢±ūĪŖĘäÖŠČżÖÖŌŖĖŲ¶ŌÓ¦µÄµ„ÖŹ£¬±ūĪŖµ»ĘÉ«¹ĢĢ壬Ņ×ČÜŌŚBD2ÖŠ£¬pµÄĖ®ČÜŅŗŹĒŅ»ÖÖ¶žŌŖČõĖį£¬ÓŠĘư׊Ō£®ÉĻŹöĪļÖŹµÄ×Ŗ»Æ¹ŲĻµČēĶ¼ĖłŹ¾£Ø·“Ó¦Ģõ¼žŹ”ĀŌ£©£®ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | Ō×Ó°ė¾¶£ŗA£¼B£¼C | |
| B£® | BD2·Ö×ÓÖŠĖłÓŠŌ×Ó¶¼“ļµ½ĮĖ8µē×ÓĪČ¶Ø½į¹¹ | |
| C£® | CÓėDµÄ¼ņµ„Ēā»ÆĪļ·Šµć£¬ŗóÕßøß | |
| D£® | ·Ē½šŹōŠŌ£ŗD£¾C£¾B |
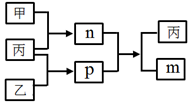
·ÖĪö ¶ĢÖÜĘŚÖ÷×åŌŖĖŲA”¢B”¢C”¢DµÄŌ×ÓŠņŹżŅĄ“ĪŌö“ó£¬CŗĶDĪ»ÓŚĶ¬Ņ»Ö÷×壮m”¢n”¢p¾łĪŖÓÉÕāŠ©ŌŖĖŲ×é³ÉµÄ¶žŌŖ»ÆŗĻĪļ£¬¼×”¢ŅŅ”¢±ūĪŖĘäÖŠČżÖÖŌŖĖŲ¶ŌÓ¦µÄµ„ÖŹ£¬±ūĪŖµ»ĘÉ«¹ĢĢ壬±ūĪŖS£¬Ņ×ČÜŌŚCS2ÖŠ£¬æÉÖŖBĪŖCŌŖĖŲ£¬DĪŖSŌŖĖŲ£»pµÄĖ®ČÜŅŗŹĒŅ»ÖÖ¶žŌŖČõĖį£¬ÓŠĘư׊Ō£¬pĪŖSO2£¬½įŗĻĶ¼ÖŠ×Ŗ»ÆæÉÖŖ£¬ŅŅĪŖO2£¬¼×ĪŖH2£¬n+p=m+±ū£¬nĪŖŅŌÉĻŌŖĖŲŠĪ³ÉµÄ¶žŌŖ»ÆŗĻĪļ£¬ŌņnĪŖH2S£¬mĪŖH2O£¬½įŗĻŌ×ÓŠņŹżæÉÖŖ£¬AĪŖHŌŖĖŲ£¬CĪŖOŌŖĖŲ£¬ŅŌ“ĖĄ“½ā“š£®
½ā“š ½ā£ŗÓÉÉĻŹö·ÖĪöæÉÖŖ£¬AĪŖH£¬BĪŖC£¬CĪŖO£¬DĪŖS£¬
A£®µē×Ó²ćŌ½¶ą£¬Ō×Ó°ė¾¶Ō½“ó£¬Ķ¬ÖÜĘŚ“Ó×óĻņÓŅŌ×Ó°ė¾¶¼õŠ”£¬ŌņŌ×Ó°ė¾¶Ó¦ĪŖA£¼C£¼B£¬¹ŹA“ķĪó£»
B£®BD2ĪŖCS2£¬µē×ÓŹ½ĪŖ £¬ĖłŅŌŌ×Ó¶¼“ļµ½8µē×ÓĪČ¶Ø½į¹¹£¬¹ŹBÕżČ·£»
£¬ĖłŅŌŌ×Ó¶¼“ļµ½8µē×ÓĪČ¶Ø½į¹¹£¬¹ŹBÕżČ·£»
C£®CÓėDµÄ¼ņµ„Ēā»ÆĪļ·Ö±šĪŖH2OŗĶH2S£¬H2O·Ö×Ó¼ä“ęŌŚĒā¼ü·Šµć“óÓŚH2S£¬¹ŹC“ķĪó£»
D£®·Ē½šŹōŠŌÓ¦ĪŖO£¾S£¾C£¬¹ŹD“ķĪó£»
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éŌ×Ó½į¹¹ÓėŌŖĖŲÖÜĘŚĀÉ£¬ĪŖøßĘµæ¼µć£¬°ŃĪÕŌŖĖŲ»ÆŗĻĪļÖŖŹ¶”¢ĪļÖŹŠŌÖŹ”¢Ļą»„×Ŗ»ÆĄ“ĶʶĻĪļÖŹĪŖ½ā“šµÄ¹Ų¼ü£¬²ąÖŲ·ÖĪöÓėĶʶĻÄÜĮ¦µÄ漲飬עŅāĶ»ĘĘæŚŌŚ±ū”¢±ūĪŖµ»ĘÉ«µÄµ„ÖŹ£¬ĢāÄæÄŃ¶Č²»“ó£®


 ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø
ĢģĢģĻņÉĻŅ»±¾ŗĆ¾ķĻµĮŠ“š°ø Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
Š”ѧɜ10·ÖÖÓÓ¦ÓĆĢāĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | HC”ŌCH | B£® | CH2ØTCH2 | C£® | CH3-C”ŌCH | D£® | CH2ØTC£ØCH3£©2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ¶ąŃ”Ģā
| A£® | ŅŃÖŖI3-?I2+I-£¬ĻņŹ¢ÓŠKI3ČÜŅŗµÄŹŌ¹ÜÖŠ¼ÓČėŹŹĮæCCl4£¬Õńµ“¾²ÖĆŗóCCl4²ćĻŌ×ĻŗģÉ«£¬ĖµĆ÷KI3ŌŚCCl4ÖŠµÄČܽā¶Č±ČŌŚĖ®ÖŠµÄ“ó | |
| B£® | ŹŅĪĀĻĀĻņ10mL pH=3µÄ“×ĖįČÜŅŗÖŠ¼ÓĖ®Ļ”ŹĶŗó£¬ČÜŅŗÖŠ$\frac{{c£ØC{H_3}CO{O^-}£©}}{{c£ØC{H_3}COOH£©•c£ØO{H^-}£©}}$¼õŠ” | |
| C£® | ŹŅĪĀŹ±ka£ØHF£©=3.6”Į10-4£¬ka£ØCH3COOH£©=1.75”Į10-5£¬0.1 mol/LµÄNaFČÜŅŗÓė0.1 mol/LµÄCH3COOKČÜŅŗĻą±Č£¬Ņ»¶ØÓŠc£ØNa+£©-c£ØF-£©£¼c£ØK+£©-c£ØCH3COO-£©³ÉĮ¢ | |
| D£® | ŌŚ25”ꏱ£¬½«0.01 mol/LµÄ°±Ė®Óė0.01 mol/LµÄŃĪĖį»ģŗĻ£¬³ä·Ö·“Ó¦ŗóČÜŅŗÖŠČōc£ØNH4+£©=c£ØCl-£©£¬Ōņ°±Ė®ĖłÓƵÄĢå»żŅ»¶Ø“óÓŚŃĪĖįµÄĢå»ż |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ö»ŗ¬ÓŠ2øöĖ«¼üµÄÖ±Į“ÓŠ»śĪļ | B£® | ŗ¬1øöĖ«¼üµÄÖ±Į“ÓŠ»śĪļ | ||
| C£® | ŗ¬1øöĖ«¼üµÄ»·×“ÓŠ»śĪļ | D£® | ŗ¬Ņ»øöČż¼üµÄÖ±Į“ÓŠ»śĪļ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | XŗĶYŠĪ³ÉµÄ»ÆŗĻĪļÖŠŅ»¶Ø²»ŗ¬¹²¼Ū¼ü | |
| B£® | WµÄŃõ»ÆĪļµÄĖ®»ÆĪļŹĒĒæĖį | |
| C£® | ZX2ÄÜŹ¹ĖįŠŌKMnO4ČÜŅŗĶŹÉ«£¬ĖµĆ÷ZX2¾ßÓŠĘư׊Ō | |
| D£® | XŗĶZµÄ¼ņµ„Ēā»ÆĪļ·Šµć²īŅģ“ó£¬Ö÷ŅŖŌŅņŹĒĒā¼üµÄÓ°Ļģ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | CSOµÄµē×ÓŹ½£ŗ | |
| B£® | Cl-µÄ½į¹¹Ź¾ŅāĶ¼£ŗ | |
| C£® | Ō×ÓŗĖÄŚÓŠ20øöÖŠ×ÓµÄĀČŌ×Ó£ŗ${\;}_{17}^{20}$Cl | |
| D£® | ±½·Ö×ÓµÄĒņ¹÷Ä£ŠĶ£ŗ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | NH4HCO3ŗĶŃĪĖįµÄ·“Ó¦ŹĒ·ÅČČ·“Ó¦ | |
| B£® | øĆ·“Ó¦ÖŠ£¬ČČÄÜ×Ŗ»ÆĪŖ²śĪļÄŚ²æµÄÄÜĮæ | |
| C£® | ·“Ó¦ĪļµÄ×ÜÄÜĮæøßÓŚÉś³ÉĪļµÄ×ÜÄÜĮæ | |
| D£® | ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ĪŖNH4HCO3+HCl”śNH4Cl+CO2”ü+H2O”÷H=+Q kJ•mol-1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com