
A、B、C三种强电解质,它们在水中电离出的离子如下表所示:
| 阳离子 | Ag+ Na+ |
| 阴离子 | NO3- SO42- Cl- |


(1)负 NaCl;(2)2H2O 2H2↑+O2↑; (3) M; (4) SO2+2H2O-2e-=4H++SO42-
2H2↑+O2↑; (3) M; (4) SO2+2H2O-2e-=4H++SO42-
解析试题分析:(1)因为Ag+会与SO42-、Cl-发生离子反应产生沉淀,所以只能是AgNO3溶液。则另外的两种电解质溶液分别是Na2SO4、NaCl溶液。由于乙烧杯C电极增重,则乙烧杯的溶液为AgNO3溶液。C电极增重说明C为阴极,直流电源电极M为负极,N为正极。AgNO3溶液电解的方程式为:4AgNO3+2H2O 4Ag+O2↑+4HNO3.随着电解的进行,溶液的酸性逐渐增强。(2)由于丙溶液在电解的过程中溶液的PH不变,所以实质上是电解水。应该是活泼金属的含氧酸盐。丙溶液为Na2SO4。电解的方程式为2H2O
4Ag+O2↑+4HNO3.随着电解的进行,溶液的酸性逐渐增强。(2)由于丙溶液在电解的过程中溶液的PH不变,所以实质上是电解水。应该是活泼金属的含氧酸盐。丙溶液为Na2SO4。电解的方程式为2H2O 2H2↑+O2↑则甲溶液为NaCl。电解的方程式为2NaCl+2H2O
2H2↑+O2↑则甲溶液为NaCl。电解的方程式为2NaCl+2H2O Cl2↑+H2↑+2NaOH。(3)若用如图所示Zn-Cu原电池作直流电源,则活动性较强的Zn作电源的负极相当于直流电源的M极。(4)若用图二所示装置做直流电源,不仅可以完成电解也能将气体SO2转化为重要化工原料。根据如图所说的装置可知SO2被氧化为H2SO4,所以通入SO2气体的电极为负极,电极反应式为SO2+2H2O-2e-=4H++SO42-。通入O2的电极为正极,电极反应式为O2+4e-+4H+=2H2O。
Cl2↑+H2↑+2NaOH。(3)若用如图所示Zn-Cu原电池作直流电源,则活动性较强的Zn作电源的负极相当于直流电源的M极。(4)若用图二所示装置做直流电源,不仅可以完成电解也能将气体SO2转化为重要化工原料。根据如图所说的装置可知SO2被氧化为H2SO4,所以通入SO2气体的电极为负极,电极反应式为SO2+2H2O-2e-=4H++SO42-。通入O2的电极为正极,电极反应式为O2+4e-+4H+=2H2O。
考点:考查电源的电极的判断、盐溶液的电解原理及特点与原电池、电解池的电极反应式的书写的知识。


科目:高中化学 来源: 题型:填空题
电极a、b分别为Ag电极和Pt电极,电极c、 d都 是 石墨电极。通电一段时间后,在c、d两极上共收集到336mL(标准状态)气体。回答:
(1)直流电源中,M为______________极。
(2)Pt电极上生成的物质是____________,其质量为____________g 。
(3)电子转移的物质的量与电极b、c、d分别生成的物质的物质的量之比为________。
(4)电解过程中,AgNO3溶液的浓度______________(填“增大”、“减小”或“不变”,
下同),AgNO3溶液的pH__________,H2SO4溶液的浓度_________ ,H2SO4溶液的pH________ 。
(5)若H2SO4溶液的质量分数由5.00%变为5.02%,则原有5.00%的H2SO4溶液为______g。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如图。
(1)电源的负极为________(填“A”或“B”)。
(2)阳极室中发生的反应依次为___________________________________、
___________________________________________________________。
(3)电解结束后,阴极室溶液的pH与电解前相比将________;若两极共收集到气体13.44 L(标准状况),则除去的尿素为________g(忽略气体的溶解)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
海洋资源的开发与利用具有广阔的前景。海水的pH一般在7.5~8.6之间。某地海水中主要离子的含量如下表:
| 成分 | Na+ | K+ | Ca2+ | Mg2+ | Cl- | S | HC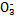 |
| 含量/(mg·L-1) | 9 360 | 83 | 200 | 1 100 | 16 000 | 1 200 | 118 |
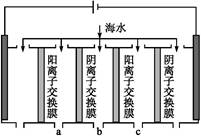
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
下图是一个化学过程的示意图,回答下列问题: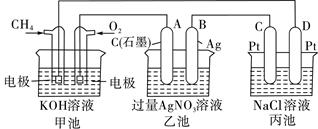
(1)甲池是 装置,电极A的名称是 。
(2)甲装置中通入CH4的电极反应式为 ,乙装置中B(Ag)的电极反应式为 ,丙装置中D极的产物是 (写化学式),
(3)一段时间,当丙池中产生112mL(标准状况下)气体时,均匀搅拌丙池,所得溶液在25℃ 时的pH =__________。(已知:NaCl溶液足量,电解后溶液体积为500 mL)。
若要使丙池恢复电解前的状态,应向丙池中通入 (写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
迄今为止,由化学能转变的热能或电能仍然是人类使用的主要的能源。
I.请仔细观察下列两种电池的构造示意图,完成下列问题:
(1)碱性锌锰电池比普通锌锰电池(干电池)性能好,放电电流大。试从影响反应速率的因素分析其原因是 。
(2)碱性锌锰电池的总反应式:Zn+2MnO2+2H2O=2MnOOH+Zn(OH)2,则负极的电极反应式为 。
Ⅱ.下面是一个将化学能与电能相互转化的装置。回答下列问题:
(1)写出通入O2一极的电极反应方程式为 。
(2)a电极是 极,能否写出其电极反应方程式 (填“能”或“不能”),若“能”写出其电极反应方程式,若“不能”说明其理由 。
(3)下列说法不正确的是( )
| A.此装置用于电镀铜时,电解一段时间,硫酸铜溶液的浓度不变 |
| B.U型管中,OH—在a极放电 |
| C.若a为纯净金属,b为粗制金属,该装置可用于粗制金属的精炼 |
| D.电子经导线流入b电极 |

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
按下图装置进行实验,并回答下列问题
(1)判断装置的名称:A池为
(2)锌电极反应式为__________________
石墨棒C1为______极,电极反应式为__________
石墨棒C2附近发生的实验现象为______________
(3)当C2极析出2.24L气体(标准状态)时,锌的质量减少了__g.CuSO4溶液的质量增加了______g
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
钠及其化合物具有广泛的用途。 (1)工业上可利用反应Na(1)+ KCl(1) K(g)+ NaCl(1)来治炼金属钾,此反应利用了钠的还原性及___ _____,
(1)工业上可利用反应Na(1)+ KCl(1) K(g)+ NaCl(1)来治炼金属钾,此反应利用了钠的还原性及___ _____,
写出钠与TiCl4反应冶炼Ti的化学方程式______________ _______。
(2)用Na2CO3熔融盐作电解质,CO、O2为原料组成的新型电池的研究取得了重大突破。该电池示意图如图:
负极电极反应式为________________,为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环。A物质的化学式为______________。
(3)Li-SOCl2电池可用于心脏起搏器。该电池的电极材料分别为锂和碳,电解液是
LiAlCl4-SOCl2。电池的总反应可表示为: 4Li + 2SOCl2 =4LiCl + S + SO2。
请回答下列问题:
①电池的负极材料为 ,发生的电极反应为 ;
②电池正极发生的电极反应为 ;
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
某厂废水中含量金属Cr3+(含有少量Fe3+、Cu2+)。某研究性学习小组为了变废为宝,将废水处理得到重铬酸钾。某含铬废水处理的主要流程如图所示:
已知:① 沉淀完全,而在pH≥3.2时
沉淀完全,而在pH≥3.2时
Fe(OH)3沉淀完全。
②CrO2—4在酸性环境中发生:
回答下列问题:
(1)滤渣的成分是 。(写化学式)
(2)写出第③步反应的离子方程式 。
(3)分离出含[Cr(OH)4]—的溶液需要的玻璃仪器有 。
(4)目前一种采用以铬酸钾为原料,电化学法制备重要铬酸钾的实验装置示意图如下:
电解一段时间后,测定阳极液中K元素和Cr元素的含量,若K元素与Cr元素的物质的量之比 为d,则此时的铬酸钾的转化率为 。
为d,则此时的铬酸钾的转化率为 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com