
| 元素 电离能/kJ•mol-1 | X | Y | Z |
| I1 | 496 | 738 | 577 |
| I2 | 4 562 | 1 451 | 1 817 |
| I3 | 6 912 | 7 733 | 2 754 |
| I4 | 9 540 | 10 540 | 11 578 |
| A. | 三种元素中,X元素的第一电离能最小,其电负性在同一周期元素中也最小 | |
| B. | 三种元素中,Y元素的第一电离能最大,其电负性也最大 | |
| C. | 等物质的量的X、Y、Z三种单质与少量盐酸反应时放出的氢气的物质的量之比为1:1:1 | |
| D. | 三种单质与盐酸反应放出等量氢气时,消耗X、Y、Z的物质的量之比为3:2:1 |
分析 根据元素电离能的变化知,X为第ⅠA族元素、Y为第ⅡA族元素、Z为第ⅢA族元素,又X、Y、Z为同一周期的三种元素,而且X为第ⅠA族元素可以失去4个电子,则这几种元素为第三周期,分别是Na、Mg、Al元素;
A、根据第一电离能数据判断最小的为X(Na),根据同周期从左向右电负性逐渐增大,判断电负性最小的元素;
B、根据第一电离能数据判断最大的为Y(Mg),根据同周期从左向右电负性逐渐增大,判断电负性最大的元素;
C、相同物质的量的钠、镁、铝与少量盐酸反应,盐酸完全反应,根据氢守恒所以与盐酸反应生成的氢气相等,但钠还可以与水反应生成氢气,则最终钠生成的氢气最多,镁和铝相等;
D、根据三种金属的化合价可得与盐酸反应的关系式分别为:2Na~H2,Mg~H2,$\frac{2}{3}$Al~H2,根据反应的方程式计算.
解答 解:根据元素电离能的变化知,X为第ⅠA族元素、Y为第ⅡA族元素、Z为第ⅢA族元素,又X、Y、Z为同一周期的三种元素,而且X为第ⅠA族元素可以失去4个电子,则这几种元素为第三周期,分别是Na、Mg、Al元素,
A、根据以上分析,X、Y、Z分别是Na、Mg、Al元素,其第一电离能最小的为X(Na),又同周期从左向右电负性逐渐增大,所以X(Na)电负性在同一周期元素中最小,故A正确;
B、根据以上分析,X、Y、Z分别是Na、Mg、Al元素,其第一电离能最大的为Y(Mg),又同周期从左向右电负性逐渐增大,所以Z(Al)电负性在同一周期元素中最大,故B错误;
C、相同物质的量的钠、镁、铝与少量盐酸反应,盐酸完全反应,根据氢守恒所以与盐酸反应生成的氢气相等,但钠还可以与水反应生成氢气,则最终钠生成的氢气最多,镁和铝相等,故C错误;
D、因Na、Mg、Al与足量的盐酸反应生成等质量的H2,由关系式:2Na~H2,Mg~H2,$\frac{2}{3}$Al~H2,得三种金属的物质的量之比为:2:1:$\frac{2}{3}$=6:3:2,故D错误;
故选:A.
点评 本题根据电离能进行推断,主要考查了第一电离能、电负性的大小判断以及有关钠、镁、铝与盐酸反应的氧化还原反应的计算,为高频考点,把握电子守恒及过量计算分析为解答的关键,侧重分析与计算能力的考查,题目难度不大.


 口算能手系列答案
口算能手系列答案科目:高中化学 来源: 题型:解答题
 X、Y、Z、R为短周期元素且原子序数依次增大.X、R原子核外电子层数等于其最外层电子数,且原子半径X<Y,Y元素的基态原子中电子分布在3个不同的能级,且每个能级中的电子总数相同;Z 的两种同素异形体都存在于大气中,对生命起着重要作用.另有M元素位于周期表的第4周期第6列.请回答下列问题:
X、Y、Z、R为短周期元素且原子序数依次增大.X、R原子核外电子层数等于其最外层电子数,且原子半径X<Y,Y元素的基态原子中电子分布在3个不同的能级,且每个能级中的电子总数相同;Z 的两种同素异形体都存在于大气中,对生命起着重要作用.另有M元素位于周期表的第4周期第6列.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
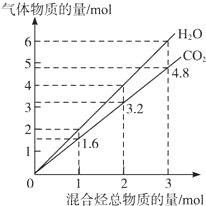 两种气态烃组成的混合气体完全燃烧后所生成CO2和H2O的物质的量随混合烃总物质的量的变化如图所示,则下列关于混合烃的判断正确的是( )
两种气态烃组成的混合气体完全燃烧后所生成CO2和H2O的物质的量随混合烃总物质的量的变化如图所示,则下列关于混合烃的判断正确的是( ) | A. | ②⑤⑥ | B. | ②⑥ | C. | ②④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
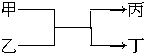 若甲、丙为短周期、同一主族元素形成的单质,乙、丁都是由两种元素组成的化合物,它们之间有如图所示的转化关系,则满足条件的甲和丙可以为( )
若甲、丙为短周期、同一主族元素形成的单质,乙、丁都是由两种元素组成的化合物,它们之间有如图所示的转化关系,则满足条件的甲和丙可以为( )| A. | ①③ | B. | ①④ | C. | ②③ | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 锡制器皿长期处于低于13.2℃的环境中,会自行毁坏 | |
| B. | 锡在常温下以灰锡状态存在 | |
| C. | 灰锡转化为白锡的反应是放热反应 | |
| D. | 灰锡和白锡的相互转化互为可逆反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验 | 除杂试剂 | 实验目的 | |
| ① | 电石与水反应 | CuSO4溶液 | 用KMnO4酸性溶液检验乙炔的还原性 |
| ② | CH3CH2Br与NaOH溶液共热 | HNO3溶液 | 用AgNO3溶液检验CH3CH2Br中的Br |
| ③ | 淀粉与稀H2SO4水浴共热 | NaOH溶液 | 用新制氢氧化铜检验水解产物的还原性 |
| ④ | C2H5OH与浓H2SO4加热至170℃ | NaOH溶液 | 用Br2的CCl4溶液证明该反应为消去反应 |
| A. | 只有①②③ | B. | 只有①②④ | C. | 只有②③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
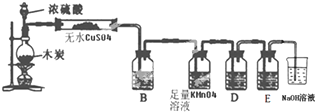
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下11.2L乙烯和丙烯的混合气体中含C-H键的数目为2NA | |
| B. | S2和S8的混合物共6.4g,其中所含硫原子数一定为0.2NA | |
| C. | 0.5mol熔融的NaHSO4中含有的离子数目为1.5NA | |
| D. | 含0.2molH2SO4的浓硫酸与足量铜反应,生成SO2的分子数为0.1NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com