

| A. | 图1表示KNO3的溶解度曲线,图中a点表示的溶液通过升温可以得到b点 | |
| B. | 图2表示某一放热反应,若使用催化剂E1、E2、△H都会发生改变 | |
| C. | 图3表示向Na2CO3和NaHCO3的混合溶液中滴加稀盐酸时,产生CO2的情况 | |
| D. | 图4表示向100 mL 0.1 mol/L的AlCl3和0.1 mol/L的NH4Cl混合溶液中滴加1 mol/L的NaOH溶液时n(Al3+)和n(AlO2-)的变化情况 |
分析 A.a点未饱和,减少溶剂可以变为饱和;
B.催化剂只能改变活化能;
C.碳酸钠先与氯化氢反应生成碳酸氢钠,开始时没有二氧化碳生成,碳酸钠反应完全之后碳酸氢钠与氯化氢反应生成二氧化碳;
D.向100 mL 0.1 mol/L的AlCl3和0.1 mol/L的NH4Cl混合溶液中滴加1 mol/L的NaOH溶液,开始先生成氢氧化铝沉淀,沉淀达到最大值,铵根离子与氢氧化钠反应,最后氢氧化铝与氢氧化钠反应.
解答 解:A.a点未饱和,减少溶剂可以变为饱和,则a点表示的溶液通过蒸发溶剂可以得到b点,故A错误;
B.加催化剂改变了反应的历程,降低反应所需的活化能,但是反应热不变,故B错误;
C.碳酸钠先与氯化氢反应生成碳酸氢钠,开始时没有二氧化碳生成,碳酸钠反应完全之后碳酸氢钠与氯化氢反应生成二氧化碳,生成二氧化碳需要的盐酸的体积大于生成碳酸氢钠消耗的盐酸,故C错误;
D.向100 mL 0.1 mol/L的AlCl3和0.1 mol/L的NH4Cl混合溶液中滴加1 mol/L的NaOH溶液,开始先生成氢氧化铝沉淀,铝离子的浓度逐渐减小,沉淀达到最大值时铝离子浓度为0,然后铵根离子与氢氧化钠反应,最后氢氧化铝与氢氧化钠反应生成偏铝酸根离子,AlO2-的物质的量逐渐增大,最后不变,故D正确.
故选D.
点评 本题考查了元素化合物的性质、溶解度、催化剂对反应的影响等,题目难度中等,侧重于考查学生的分析能力和读图能力,注意把握物质之间发生的反应.


科目:高中化学 来源: 题型:填空题
 从铁、铝合金出发的反应如图所示:
从铁、铝合金出发的反应如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
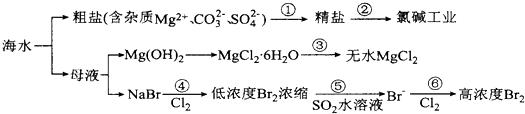
| A. | 过程①的提纯是化学过程,过程②通过氧化还原反应可产生2种单质 | |
| B. | 在过程③中将MgCl2•6H2O直接灼烧得不到MgCl2 | |
| C. | 在过程④、⑥反应中每氧化0.2 mol Br-需消耗2.24LCl2 | |
| D. | 过程⑤反应后溶液呈强酸性,生产中需解决其对设备的腐蚀问题 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,根据已有知识判定下列说法不正确的是( )
,根据已有知识判定下列说法不正确的是( )| A. | 它可使KMnO4溶液褪色 | |
| B. | 加入FeCl3溶液,能发生显色反应 | |
| C. | 它可以发生银镜反应 | |
| D. | 它被催化加氢后最终产物的化学式为C10H22O溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com