
ij����������ܺ���CaCO3��MgCl2��Na2SO4��Ba(NO3��2��CuSO4�е�һ�ֻ��֣����û�����������ʵ�飺
�ٽ�������������ˮ�еõ���ɫ��Һ�Ͱ�ɫ���������ˣ�
��ȡ��Һ������ɫ��Ӧ������ʻ�ɫ��
��ȡ��ɫ��������ϡ���ᣬ������ȫ�ܽⲢ�ų����塣
�����������ƶϣ�
��1���û������һ������ ��һ�������� �����ܺ��� ��
��2����Ҫ������ܺ��е������Ƿ���ڣ����Բ��õ�ʵ�����Ϊ ����д��ĸ����
A��ȡ���������Һ������AgNO3��Һ���ټ�ϡ����[
B��ȡ���������Һ������NaOH��Һ
C��ȡ���������Һ����������Ba(NO3��2��Һ�����ú����ϲ���Һ�м����ữAgNO3��Һ
D��ȡ���������Һ����������BaCl2��Һ�����ú����ϲ���Һ�м����ữAgNO3��Һ
 ��һ������ĩ�ٷֳ�̾�ϵ�д�
��һ������ĩ�ٷֳ�̾�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ����������������и�һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ù�����Ʒ����һ�����ʵ���Ũ�ȵ���Һ���辭���������ܽ⡢ת����Һ�����ݵȲ���������ͼʾ��Ӧ�IJ����淶����
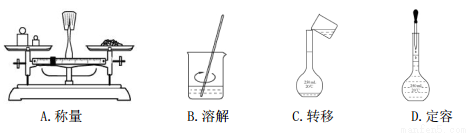
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ�����ʡ��һ��10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
������ȼ���ױ����ж��Ļ�ѧ���ʣ������������װ��������Σ�վ����ǩ���������е����ʣ������˰�װ��ǩ���ǣ� ��
| A | B | C | D |
���� | �������� | ���Ȼ�̼ | ������ | �̻����� |
�� |
|
|
|
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ�����и߶��������Ļ�ѧ�� �������棩 ���ͣ�ѡ����
������������ͬ���칹����ǣ� ��
A����ѿ�Ǻ����� B�������ʺͰ����� C���ͺ�֬ D�����ۺ���ά��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ʡ�����и߶��������Ļ�ѧ�� �������棩 ���ͣ�ѡ����
�������Һ�м���������ϡ���ᣬ����ʹ֮����ˮ�⣬Ϊ�ⶨˮ��̶ȣ���Ҫ���������Լ��еĢ� NaOH��Һ���� ������Һ���� ���Ƶ�Cu��OH��2����Һ���� ��ˮ���� BaCl2��Һ�������ȷ���ǣ� ��
A���٢� B���ڢ� C���٢ڢ� D���ڢۢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���㽭ʡ��һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
100gŨ��Ϊ13.6 mol��L��1 HNO3���ѣ�1 g��cm��3���м���A gˮ��Ũ�ȱ�Ϊ 6.8 mol��L��1�������ˮ�����
A����100 mL B��=100 mL C����100 mL D������ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���㽭ʡ��һ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����й�ʵ�������˵����ȷ����
A. ��������ʱ��Ӧʹ������е�ˮ����ȫ���ɺ���ֹͣ����
B. ���鰱��ʱ�����ò�����մȡʪ��ĺ�ɫʯ����ֽ�������ܿ�
C. ��ϡ������Һϴ�Ӳ����ղ�˿���ٽ�����ɫ��Ӧ
D. ��CCl4��ȡ��ˮ�е��壬��Һʱ�л���ӷ�Һ©�����Ͽڵ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ���㽭ʡ�߶������л�ѧ�Ծ��������棩 ���ͣ������
�¿���Ϊ�����������ȼ�ϣ���N2O4��Ӧ����N2��ˮ��������֪��
��N2(g)+2O2(g)��N2O4(l)��H1����19.5kJ��mol��1
��N2H4(l)+O2(g)��N2(g)+2H2O(g)��H2����534.2kJ��mol��1
��1��д���º�N2O4��Ӧ����N2��ˮ�������Ȼ�ѧ����ʽ___________________��
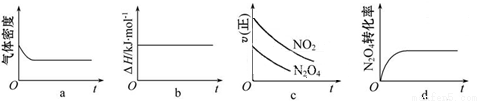
��2������к��г��ֺ���ɫ���壬���¶�����ʱ��������ɫ���ԭ���Ǵ������·�Ӧ��N2O4(g) 2NO2(g) ��H��0��һ���¶��£���1 mol N2O4 ����һ��ѹ�ܱ������з���������Ӧ������ʾ��ͼ��ȷ����˵����Ӧ�ﵽƽ��״̬���� ��
2NO2(g) ��H��0��һ���¶��£���1 mol N2O4 ����һ��ѹ�ܱ������з���������Ӧ������ʾ��ͼ��ȷ����˵����Ӧ�ﵽƽ��״̬���� ��
��3���¡�����ȼ�ϵ����һ�ּ���ȼ�ϵ�أ��������Һ��20%��30%��KOH��Һ���¡�����ȼ�ϵ�طŵ�ʱ�����ĵ缫��Ӧʽ�� ��
��4����ͳ�Ʊ��µķ���������NaClO����NH3���Ƶ��µ�ϡ��Һ���÷�Ӧ�����ӷ���ʽ�� ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016-2017ѧ��ɽ��ʡ�߶���10���¿���ѧ���������棩 ���ͣ�ѡ����
S����б����S�����������������ͬ����������֪��
��S(���s)��O2(g)=SO2(g) ��H1����297.16kJ��mol-1
��S(������s)��O2(g)=SO2(g) ��H2����296.83kJ��mol-1
��S(���s)=S(������s) ��H3
��S(������s)=S(g) ��H4
��S(���s)=S(g) ��H5
����˵����ȷ����
A����б��ת��Ϊ��������Ҫ���� B����б����������ȶ�
C����H4����H5 D����H4��0
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com