

| A、向CaCl2溶液中通入CO2至过量 |
| B、向澄清石灰水中通入CO2至过量 |
| C、向Na2SiO3溶液中通入CO2至过量 |
| D、AlCl3溶液滴加NaOH溶液至过量 |


 轻巧夺冠周测月考直通名校系列答案
轻巧夺冠周测月考直通名校系列答案科目:高中化学 来源: 题型:
| A、苯分子呈平面正六边形,六个碳碳键完全相同,键角皆为120° |
| B、苯分子中的碳原子采取sp2杂化,6个碳原子中未参与杂化的2p轨道以“肩并肩”形式形成一个大π键 |
| C、苯分子中的碳碳键是介于单键和双键之间的一种特殊类型的键 |
| D、苯能使溴水褪色,是因为苯将Br2还原为Br- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、③⑤⑥⑦⑧ | B、②③④⑥⑦ |
| C、③⑥⑧ | D、①③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、AlCl3溶液中加入过量氨水 |
| B、Al2(SO4)3溶液中加入过量KOH溶液 |
| C、FeCl2溶液中加入过量氨水 |
| D、Ca(OH)2溶液中通入过量SO2气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 往AlCl3溶液中逐滴加入NaOH溶液至过量 |
B、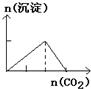 往澄清石灰水中缓慢通入CO2气体至过量 |
C、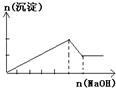 往含MgCl2、AlCl3各1mol的混合溶液中逐滴加入NaOH溶液至过量 |
D、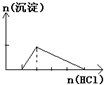 往NaOH和NaAlO2混合溶液中逐滴加入盐酸至过量 |
查看答案和解析>>
科目:高中化学 来源: 题型:
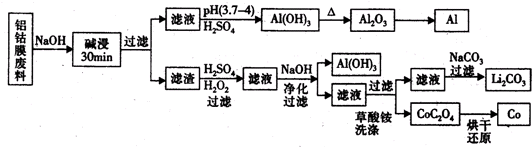
查看答案和解析>>
科目:高中化学 来源: 题型:
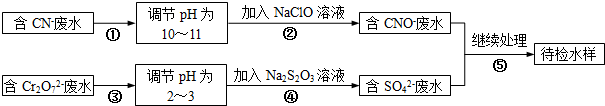
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com