
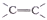 ⑥-C6H5 ⑦Br-⑧-COOH 其中不是官能团的是( )
⑥-C6H5 ⑦Br-⑧-COOH 其中不是官能团的是( )| A、①③⑤⑧ | B、②④⑦ |
| C、②③⑤⑦⑧ | D、②④⑥⑦ |
科目:高中化学 来源: 题型:
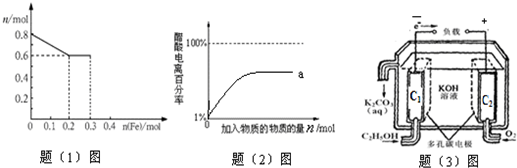
| 醋酸浓度(mol?L-1) | 1 | 0.1 | 0.01 |
| pH值 | 2.50 | 3.00 | 3.50 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、FeCl2 |
| B、CuSO4 |
| C、Na2CO3 |
| D、Ba(NO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Na+、H+、NO3-、SO32- |
| B、K+、H+、SO42-、CH3COO- |
| C、Mg2+、NH4+、SO42-、Cl- |
| D、K+、Fe3+、Cl-、SCN- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2可使酸性高锰酸钾褪色 | SO2有漂白性 |
| B | 浓硫酸具有脱水性和强氧化性 | 浓硫酸滴到湿润的蔗糖中,蔗糖变 成黑色海绵状 |
| C | SiO2有导电性 | SiO2可用于制备光导纤维 |
| D | BaSO4饱和溶液中加入饱和Na2CO3溶液有白色沉淀 | Ksp(BaSO4)<Ksp(BaCO3) |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、利用太阳能等清洁能源代替化石燃料,有利于节约资源、保护环境 |
| B、水电站把机械能转化成电能,而核电站把化学能转化成电能 |
| C、在医院中,为酸中毒病人输液应采用0.9%氯化铵溶液 |
| D、棉、麻、丝、毛及合成纤维完全燃烧都只生成CO2和H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
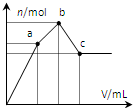 向100mL 0.1mol?L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol?L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.下列说法正确的( )
向100mL 0.1mol?L-1硫酸铝铵[NH4Al(SO4)2]溶液中逐滴滴入0.1mol?L-1 Ba(OH)2溶液.随着Ba(OH)2溶液体积V的变化,沉淀总物质的量n的变化如图所示.下列说法正确的( )| A、a点的溶液呈中性 |
| B、a点沉淀的质量比c点沉淀的质量大 |
| C、b点加入Ba(OH)2溶液的体积为250 mL |
| D、至c点完成反应,反应的离子方程式可表示为:Al3++2SO42-+NH4++2Ba2++5OH-→AlO2-+2BaSO4↓+NH3?H2O+2H2O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com