
久置的硝酸呈黄色,如何除去?怎样保存硝酸?
科目:高中化学 来源: 题型:
甲烷是天然气的主要成分,是生产生活中应用非常广泛的一种化学物质。
(1)一定条件下,用甲烷可以消除氮氧化物(NOx)的污染。已知:
CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH1
CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH2
现有一份在相同条件下对H2的相对密度为17的NO与NO2的混合气体,用16 g甲烷气体催化还原该混合气体,恰好生成氮气、二氧化碳气体和水蒸气,共放出1042.8 kJ热量。
①该混合气体中NO和NO2的物质的量之比为________。
②已知上述热化学方程式中ΔH1=-1160 kJ/mol,则ΔH2=________。
③在一定条件下NO气体可以分解为NO2气体和N2气体,写出该反应的热化学方程式:______________。
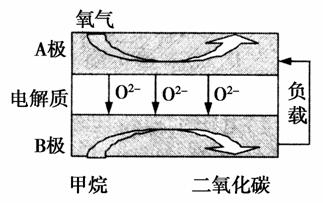
(2)以甲烷为燃料的新型电池,其成本大大低于以氢气为燃料的传统燃料电池,目前得到广泛地研究,如图是目前研究较多的一类固体氧化物燃料电池工作原理示意图。回答下列问题:
④B极为电池________极,电极反应式为________________。
⑤若用该燃料电池作电源,用石墨作电极电解100 mL 1 mol/L的硫酸铜溶液,写出阳极的电极反应式:_______________,当两极收集到的气体体积相等时,理论上消耗的甲烷的体积为______(标准状况下),实际上消耗的甲烷体积(折算到标准状况)比理论上大,可能原因为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知:CO(g)+H2O(g)CO2(g)+H2(g) ΔH=Q,其平衡常数随温度变化如下表所示:
| 温度/℃ | 400 | 500 | 850 |
| 平衡常数 | 9.94 | 9 | 1 |
请回答下列问题:
(1)上述反应的化学平衡常数表达式为:________________。该反应的Q________________0(填“>”或“<”)。
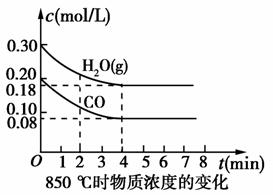
(2)850 ℃时在体积为10 L反应器中,通入一定量的CO和H2O(g),发生上述反应,CO和H2O(g)浓度变化如图所示,则0~4 min时平均反应速率v(CO)=________。
(3)若在500 ℃时进行,且CO、H2O(g)的起始浓度均为0.020 mol/L,该条件下,CO的最大转化率为________________。
(4)若在850 ℃时进行,设起始时CO和H2O(g)共为1 mol,其中水蒸气的体积分数为x,平衡时CO的转化率为y,试推导y随x变化的函数关系式为________________。
(5)某电化学装置可实现2CO2===2CO+O2的转化,使CO重复使用。已知该反应的阳极反应为4OH--4e-===2H2O+O2↑,则阴极反应式为________________。
(6)有人提出可以设计反应2CO===2C+O2(ΔH>0)来消除CO的污染。请判断上述反应能否自发进行:________________(填“可能”或“不可能”),理由是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
铜与一定量浓硝酸反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,这些气体与5.6 L O2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸。则消耗铜的质量为 ( )
A.16 g B.32 g C.64 g D.无法计算
查看答案和解析>>
科目:高中化学 来源: 题型:
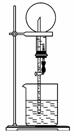 右图的装置中,干燥烧瓶内盛有某种气体,烧杯和滴管内盛放某种溶液。挤压滴管的胶头,下列与实验事实不相符的是 ( )
右图的装置中,干燥烧瓶内盛有某种气体,烧杯和滴管内盛放某种溶液。挤压滴管的胶头,下列与实验事实不相符的是 ( )
A.CO2(NaHCO3溶液)/无色喷泉
B.NH3(H2O中含酚酞)/红色喷泉
C.H2S(CuSO4溶液)/黑色喷泉
D.HCl(AgNO3溶液)/白色喷泉
查看答案和解析>>
科目:高中化学 来源: 题型:
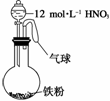 如图所示,向一定量的铁粉中加入一定体积12 mol·L-1的硝酸,加热充分反应后,下列微粒在体系中一定大量存在的是 ( )
如图所示,向一定量的铁粉中加入一定体积12 mol·L-1的硝酸,加热充分反应后,下列微粒在体系中一定大量存在的是 ( )
①NO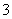 ②Fe3+ ③H+ ④NO ⑤NO2
②Fe3+ ③H+ ④NO ⑤NO2
A.① B.①⑤
C.②④⑤ D.①②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
[化学—选修2化学与技术](15分)
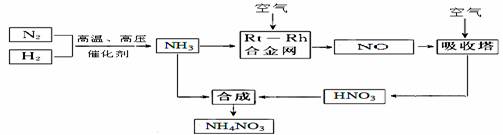 硝酸铵在现代农业生产和国防中都占有重要地位,下图是云南天然气化工厂合成硝酸铵的简要生产工艺流程:
硝酸铵在现代农业生产和国防中都占有重要地位,下图是云南天然气化工厂合成硝酸铵的简要生产工艺流程:
回答下列问题:
(1)N2的电子式 ,合成氨的反应中,若生成1g氨放出热量a KJ,写出该反应的热化学方程式 。
(2)氨催化氧化的化学方程式是 ,
试从化学反应速率和化学平衡原理分析温度、压强对合成氨反应的影响
。
(3)若输送NH3的管道某处发生泄漏,检测的简单方法
。
(4)农业生产上长期、过量使用化肥硝酸铵,会加重土壤酸化,原因是(用离子方程式回答) 。
(5)25℃时,将x mol NH4NO3溶于一定量水中,向该溶液中滴加y L氨水后溶液呈中性,则滴加氨水过程中水的电离平衡将 (填“正向” “不”或“逆向”)移动,所滴加氨水的物质的量浓度为 (25℃时,Kb(NH3·H2O)=2.0 × 10-5 mol·L-1)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com