
ŅŃÖŖ2H2(g)+O2(g)”ś2H2O(g)+483£®6kJ”£ĻĀĮŠĖµ·Ø»ņ±ķ“ļÕżČ·µÄŹĒ
| A£®ŌŚĻąĶ¬µÄĢõ¼žĻĀ£¬2mol ĒāĘųÓė 1 mol ŃõĘųµÄ×ÜÄÜĮæŠ”ÓŚ2mol Ė®ÕōĘųµÄ×ÜÄÜĮæ |
| B£®H2(g)+1/2 O2(g)”śH2O(1)+Q1£»Q1£¾241£®8kJ |
| C£®H2(g)+ 1/2O2(g)”śH2O(1)+Q2£»Q2£¼241£®8kJ |
| D£®ČĪŗĪĢõ¼žĻĀ£¬2LĖ®ÕōĘų·Ö½ā³É2LĒāĘųÓė1LŃõĘųŠčĪüŹÕ483£®6kJČČĮæ |
 Ņ»æĪŅ»Į·æĪŹ±“ļ±źĻµĮŠ“š°ø
Ņ»æĪŅ»Į·æĪŹ±“ļ±źĻµĮŠ“š°ø ĘŚÄ©±¦µäµ„ŌŖ¼ģ²ā·ÖĄąø“Ļ°¾ķĻµĮŠ“š°ø
ĘŚÄ©±¦µäµ„ŌŖ¼ģ²ā·ÖĄąø“Ļ°¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĶźČ«Č¼ÉÕŅ»¶ØÖŹĮæµÄĪŽĖ®ŅŅ“¼£¬·Å³öµÄČČĮæĪŖQ£¬ĪŖĶźČ«ĪüŹÕÉś³ÉµÄCO2£¬²¢Ź¹Ö®Éś³ÉÕżŃĪNa2CO3£¬Ļūŗĵō0.8mol£ÆL NaOHČÜŅŗ500mL£¬ŌņČ¼ÉÕ1mol¾Ę¾«·Å³öµÄČČĮæŹĒ
| A£®0.2Q | B£®0.1Q | C£®5Q | D£®10Q |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠ±ä»Æ¹ż³Ģ£¬ŹōÓŚ·ÅČČ¹ż³ĢµÄŹĒ
| A£®ŅŗĢ¬Ė®±ä³ÉĖ®ÕōĘų | B£®Ėį¼īÖŠŗĶ·“Ó¦ |
| C£®ČõĖįµēĄė | D£®NH4Cl¾§ĢåÓėBa(OH)2”¤8H2O»ģŗĻ½Į°č |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ij·ĻĖ®“¦Ąķ³§“¦Ąķ·ĻĖ®ÖŠNH+µÄ¹ż³ĢČēĻĀ£ŗ
¢ŁNH4+(aq)+ O2(g)=HNO2(aq)+H+(aq)+H2O(1) ¦¤H="-b" KJ/mol
O2(g)=HNO2(aq)+H+(aq)+H2O(1) ¦¤H="-b" KJ/mol
¢Ś2HNO2(aq)+O2(g)=2NO3-(aq)+2H+ ¦¤H=-aKJ/mol
ĻĀĮŠŠšŹöÕżČ·µÄŹĒ( )
| A£®½«NH4+×Ŗ»ÆĪŖNO3-µÄČČ»Æѧ·½³ĢŹ½æɱķŹ¾ĪŖ£ŗ NH4+(aq)+2O2(g)=NO3-(aq)+2H+(aq)+H2O(1)¦¤H=-(b+  )KJ/mol )KJ/mol |
| B£®ŌŚÉĻŹöĮ½“Ī×Ŗ»Æ¹ż³ĢÖŠ£¬·ĻĖ®µÄĖįŠŌĻČŌö“óČ»ŗóÖš½„¼õČõ |
| C£®³£ĪĀĻĀ£¬ČōHNO3ČÜŅŗÖŠc(H+)="0.1" mol”¤L-1£¬ŌņøĆČÜŅŗµÄpH>1 |
| D£®ČōÉĻŹöĮ½“Ī×Ŗ»ÆĶźČ«£¬²»æ¼ĀĒĘäĖüŌÓÖŹĄė×ӵēęŌŚ£¬Ōņ£ŗc(NH4+)+c(OH-)=c(NO3-)+c(H+) |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ŃŠÖĘŗĶæŖ·¢²»ŗ¬Ģ¼²¢æɹ¤ŅµÉś²śµÄĒå½ąÄÜŌ“£¬Ņ»Ö±ŹĒæĘѧ¼Ņ²»Šø×·ĒóµÄÄæ±ź£¬ÄæĒ°Ņŗ°±±»ČĖĆĒŹÓĪŖŅ»ÖÖĒ±ŌŚµÄĒå½ąČ¼ĮĻ”£Ņŗ°±Č¼ÉյĻÆѧ·“Ó¦·½³ĢŹ½ĪŖ£ŗ4NH3+3O2 2N2+6H2O”£ŗĶĒāČ¼ĮĻĻą±ČÓŠ¹ŲŹż¾Ż¼ūĻĀ±ķ£¬¾Ż“ĖÅŠ¶ĻÕżČ·µÄŹĒ
2N2+6H2O”£ŗĶĒāČ¼ĮĻĻą±ČÓŠ¹ŲŹż¾Ż¼ūĻĀ±ķ£¬¾Ż“ĖÅŠ¶ĻÕżČ·µÄŹĒ
| Č¼ĮĻ | ·Šµć£Ø”ę£© | Č¼ÉÕČČ£ØkJ/mol£© | Ļą¶Ō·Ö×ÓÖŹĮæ | ŅŗĢ¬ĆÜ¶Č£Øg/cm3£© |
| Ēā | -252.6 | 238.40 | 2.02 | 0.07 |
| °± | -33.50 | 317.10 | 17.03 | 0.61 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠ¹ŲÓŚø÷Ķ¼µÄŠšŹöÖŠ£¬ÕżČ·µÄŹĒ
A£®Ķ¼¼×±ķŹ¾£±mol H2 (g)ĶźČ«Č¼ÉÕÉś³ÉĖ®ÕōĘųĪüŹÕ241.8 kJČČĮæ
B£®Ķ¼¼×±ķŹ¾2 mol H2(g)Ėł¾ßÓŠµÄÄÜĮæ±Č2 molH2O(g)Ėł¾ßÓŠµÄÄÜĮæ¶ą483.6 kJ
C£®Ķ¼ŅŅ±ķŹ¾³£ĪĀĻĀĻ”ŹĶHA”¢HBĮ½ÖÖĖįµÄĻ”ČÜŅŗŹ±£¬ČÜŅŗpHĖę¼ÓĖ®ĮæµÄ±ä»Æ£¬ŌņĶ¬ĪĀ”¢Ķ¬ÅØ¶ČµÄNaAČÜŅŗµÄpHŠ”ÓŚNaBČÜŅŗµÄpH
D£®Ķ¼ŅŅÖŠĘšŹ¼Ź±HAµÄĪļÖŹµÄĮæÅØ¶Č“óÓŚHB
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĢśŗĶĻ”ĮņĖįŌŚ³ØæŚČŻĘ÷ÖŠ½ųŠŠ·“Ó¦£ŗ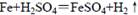 £¬ĻĀĮŠŠšŹöÖŠ²»ÕżČ·µÄŹĒ
£¬ĻĀĮŠŠšŹöÖŠ²»ÕżČ·µÄŹĒ
A£®øĆ·“Ó¦µÄ·“Ó¦¹ż³ĢÓėÄÜĮæ¹ŲĻµæÉŅŌÓĆĻĀĶ¼±ķŹ¾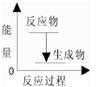 |
| B£®Čō½«øĆ·“Ó¦Éč¼Ę³ÉŌµē³Ų£¬µ±Õż¼«²śÉś22£®4LĘųĢåŹ±£¬ÓŠ56gĢśČܽā |
| C£®Čō½«øĆ·“Ó¦Éč¼Ę³ÉŌµē³Ų£¬ČÜŅŗÖŠSO42-ĻņFeµē¼«ŅĘ¶Æ |
| D£®Čō½«øĆ·“Ó¦Éč¼Ę³ÉŌµē³Ų£¬øŗ¼«·¢ÉśµÄ·“Ó¦ŹĒ£ŗFe -2e =Fe2+ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ĻĀĮŠ¹ŲÓŚ·“Ó¦¹ż³ĢÖŠÄÜĮæ±ä»ÆµÄĖµ·ØÕżČ·µÄŹĒ
| A£®Ķ¼ÖŠa”¢bĒśĻßæÉ·Ö±š±ķŹ¾·“Ó¦CH2£½CH2(g)£«H2(g)”śCH3CH3(g) ¦¤H£¼0Ź¹ÓĆŗĶĪ“Ź¹ÓĆ“ß»Æ¼ĮŹ±£¬·“Ó¦¹ż³ĢÖŠµÄÄÜĮæ±ä»Æ |
| B£®¼ŗÖŖ2C(s)£«2O2(g)£½2CO2(g) ¦¤H1£»2C(s)£«O2(g)£½2CO(g) ¦¤H2”£Ōņ¦¤H1£¾¦¤H2 |
| C£®Ķ¬ĪĀĶ¬Ń¹ĻĀ£¬·“Ó¦H2(g)£«Cl2(g)£½2HCl(g)ŌŚ¹āÕÕŗĶµćČ¼Ģõ¼žĻĀµÄ¦¤H²»Ķ¬ |
| D£®ŌŚŅ»¶ØĢõ¼žĻĀ£¬Ä³æÉÄę·“Ó¦µÄ¦¤H£½£«100kJ”¤mol£1£¬ŌņøĆ·“Ó¦Õż·“Ó¦»ī»ÆÄܱČÄę·“Ó¦»ī»ÆÄÜ“ó100kJ”¤mol£1 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗµ„Ń”Ģā
ŅŃÖŖ298 K,101 kPaŹ±£¬2SO2(g)£«O2(g)  2SO3(g)£»¦¤H£½£197 kJ”¤mol£1”£ŌŚĻąĶ¬ĪĀ¶ČŗĶŃ¹ĒæĻĀ£¬ĻņĆܱÕČŻĘ÷ÖŠĶØČė2 mol SO2ŗĶ1 mol O2£¬“ļµ½Ę½ŗāŹ±£¬·Å³öČČĮæĪŖQ1£¬ĻņĮķŅ»øöĢå»żĻąĶ¬µÄČŻĘ÷ÖŠĶØČė1 mol SO2,0.5 mol O2ŗĶ1 mol SO3£¬“ļµ½Ę½ŗāŹ±·Å³öČČĮæĪŖQ2£¬ŌņĻĀĮŠ¹ŲĻµÕżČ·µÄŹĒ(””””)
2SO3(g)£»¦¤H£½£197 kJ”¤mol£1”£ŌŚĻąĶ¬ĪĀ¶ČŗĶŃ¹ĒæĻĀ£¬ĻņĆܱÕČŻĘ÷ÖŠĶØČė2 mol SO2ŗĶ1 mol O2£¬“ļµ½Ę½ŗāŹ±£¬·Å³öČČĮæĪŖQ1£¬ĻņĮķŅ»øöĢå»żĻąĶ¬µÄČŻĘ÷ÖŠĶØČė1 mol SO2,0.5 mol O2ŗĶ1 mol SO3£¬“ļµ½Ę½ŗāŹ±·Å³öČČĮæĪŖQ2£¬ŌņĻĀĮŠ¹ŲĻµÕżČ·µÄŹĒ(””””)
| A£®Q2£¼Q1£¼197 kJ”¤mol£1 | B£®Q2£½Q1£½197 kJ”¤mol£1 |
| C£®Q1£¼Q2£¼197 kJ”¤mol£1 | D£®Q2£½Q1£¼197 kJ”¤mol£1 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com