
| A.在适当温度和催化剂作用下,用2molSO2和1molO2合成SO3 |
| B.标准状况下,将1g铝片投入20mL 18mol·L-1的硫酸中 |
| C.常温下,向100mL 3mol·L-1的硝酸中加入6.4gCu |
| D.将含有少量H2O(g)的H2通入足量Na2O2容器中并不断用电火花点燃 |
 寒假乐园北京教育出版社系列答案
寒假乐园北京教育出版社系列答案科目:高中化学 来源:不详 题型:单选题

| 选项 | 蓝 | 黑 | 红 | 黄 | 绿 |
| A | SiO2 | CuSO4溶液 | O2 | NaOH溶液 | Ag |
| B | O2 | 稀H2SO4 | CO2 | Fe | NaOH溶液 |
| C | O2 | 稀H2SO4 | Al(OH)3 | NH3 | NaOH溶液 |
| D | Mg | CO2 | KOH溶液 | Al | Fe2O3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
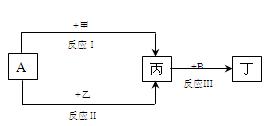
 反应。
反应。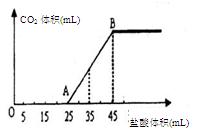
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.生成白色沉淀的离子方程式是:Mg2++2OH-="=" Mg(OH)2↓ |
| B.白色沉淀转化为红褐色沉淀的离子方程式是:3Mg(OH)2+2Fe3+==3Mg2++2Fe(OH)3 |
| C.上述实验说明Mg(OH)2的Ksp小于Fe(OH)3的Ksp |
| D.最后所得的溶液中离子浓度大小关系为: |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.⑥③④② | B.②③⑤① | C.②③④① | D.⑥①⑤③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 )错误的是
)错误的是| A.硅(半导体材料) | B.二氧化硅(制光导纤维) |
| C.水玻璃(用作粘合剂) | D.玻璃钢(用作耐火材料) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.已知反应CH4(g)+2O2(g)→CO2(g)+2H2O(1) 其△S>0 |
| B.对有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大 |
| C.在滴有酚酞的Na2CO3溶液中,逐滴加入BaCl2溶液,溶液褪色 |
| D.在高温条件下,C能置换出SiO2中的Si,说明C的氧化性强于Si |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com