
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 3 |
| 2 |


 亮点激活精编提优100分大试卷系列答案
亮点激活精编提优100分大试卷系列答案科目:高中化学 来源: 题型:
| A、Na2O |
| B、Na2CO3 |
| C、NaHCO3 |
| D、Ca(OH)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 能量是一个世界性的话题,如何充分利用能量、开发新能源,为人类服务是广大科技工作者不懈努力的目标.
能量是一个世界性的话题,如何充分利用能量、开发新能源,为人类服务是广大科技工作者不懈努力的目标.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
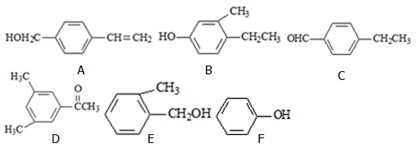
查看答案和解析>>
科目:高中化学 来源: 题型:
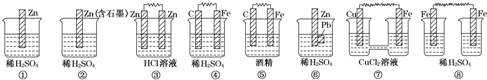
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下是气体 |
| B、常温常压下性质很稳定 |
| C、不能使酸性高锰酸钾溶液褪色 |
| D、可以使溴水褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2+H2O?H2CO3 化合反应 | ||||
B、Cu(OH)2
| ||||
C、MnO2+2CO
| ||||
| D、NaCl+AgNO3═AgCl↓+NaNO3 复分解反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com