
| A. | 甲烷的电子式: | B. | CCl4分子的比例模型: | ||
| C. | 乙烯与丁二烯的最简式相同 | D. | 2-甲基丁醇的结构简式: |
分析 A.甲烷为共价化合物,C最外层形成8个电子;
B.CCl4分子中Cl原子半径比C大;
C.乙烯与丁二烯的最简式分别为CH2、C2H3;
D. 为3-甲基丁醇.
为3-甲基丁醇.
解答 解:A.甲烷为共价化合物,C最外层形成8个电子,电子式为 ,故A正确;
,故A正确;
B.CCl4分子中Cl原子半径比C大, 为甲烷的比例模型,故B错误;
为甲烷的比例模型,故B错误;
C.乙烯与丁二烯的最简式分别为CH2、C2H3,二者最简式不同,故C错误;
D.2-甲基丁醇的结构简式为CH3CH2CH(CH3)CH2OH, 为3-甲基丁醇,故D错误.
为3-甲基丁醇,故D错误.
故选A.
点评 本题考查了比例模型、电子式结构简式等判断,为高考常见题型,侧重考查双基知识,题目难度中等,注意明确常见的化学用语的概念及正确表示方法.


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:选择题
| A. | NH4HCO3溶于过量的浓KOH溶液中:NH4++OH-═NH3↑+H2O | |
| B. | 醋酸除去水垢:2H++CaCO3═Ca2++CO2↑+H2O | |
| C. | 向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2═2 Fe3++2Br2+6 Cl- | |
| D. | 向明矾KAl(SO4)2•12H2O]溶液中滴加Ba(OH)2溶液,恰好使SO42-沉淀完全:2Al3++3SO42-+3Ba2++6OH -═2 Al(OH)3↓+3BaSO4↓ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10ml质量分数为98%的H2SO4,用10ml水稀释后,H2SO4的质量分数大于49% | |
| B. | 配制0.1mol/L的Na2CO3溶液480mL,需用500mL容量瓶 | |
| C. | 制备Fe(OH)3胶体时,将饱和FeCl3溶液滴入沸水中,边加热边搅拌,直到得到红褐色溶液 | |
| D. | 向2等份不饱和的烧碱溶液中分别加入一定量的Na2O2、和Na2O,使溶液均恰好饱和,则加入的Na2O2与Na2O的物质的量之比等于1:1(保持温度不变) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | HBr、CO2、NH3 | B. | Na2O、Na2O2、Na2S | C. | NaCl、HCl、H2O | D. | NaOH、CaCl2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg(OH)2的溶解度最小 | |
| B. | Ca(OH)2的溶解度最小 | |
| C. | AgCl的溶解度最小 | |
| D. | 同一温度下Ksp越大的溶解度也越大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SO2、SiO2、P2O5均为酸性氧化物 | |
| B. | 稀豆浆、硅酸、氯化铁溶液均为胶体 | |
| C. | 酒精、冰醋酸、草酸钾均为电解质 | |
| D. | NH4SCN、SiO2、NH3•H2O均为共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 都是非金属氧化物 | |
| B. | 都是酸性氧化物,都能与强碱溶液反应 | |
| C. | 都能溶于水且与水反应生成相应的酸 | |
| D. | SiO2可用于制光导纤维,干冰可用于人工降雨 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
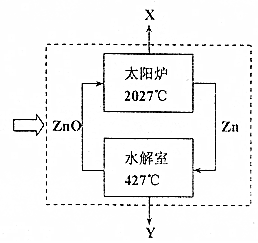
| Zn | ZnO | ZnS | CuS | BaSO4 | H2S | |
| 熔点/℃ | 419.5 | 1975(同时分解) | - | - | - | - |
| 沸点/℃ | 907 | - | - | - | - | - |
| Ksp(常温) | - | - | 2.5×10-21 | 6.4×10-35 | 1.1×10-10 | K1=1.1×10-7 K2=1.3×10-13 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com