
| A. | 1种 | B. | 2种 | C. | 3种 | D. | 4种 |
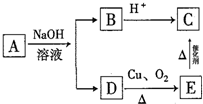
分析 A能在碱性条件下反应生成B和D,B与酸反应得到C,D连续发生氧化反应得到C,则A为酯,C为羧酸、D为醇,且C、D含有相同碳原子数目,结合A的分子式可知,C为CH3CH2COOH,D为1-丙醇,根据丙醇的可能结构判断A的结构.
解答 解:A能在碱性条件下反应生成B和D,B与酸反应得到C,D连续发生氧化反应得到C,则A为酯,C为羧酸、D为醇,且C、D含有相同碳原子数目,结合A的分子式可知,C为CH3CH2COOH,D为HOCHCH2CH3,故A的结构简式有:CH3CH2COOCHCH2CH3,故选A.
点评 本题考查有机物的推断,题目难度不大,注意根据D连续发生氧化反应生成C进行判断.


 活力课时同步练习册系列答案
活力课时同步练习册系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
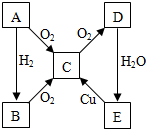 A、B、C、D、E各物质的转化关系如图所示.
A、B、C、D、E各物质的转化关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下都可用锌制容器贮存 | B. | 常温下都能与铜较快反应 | ||
| C. | 露置于空气中,溶液质量均减轻 | D. | 露置于空气中,溶液浓度均降低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表是元素按原子序数从小到大从左到右排列而成的 | |
| B. | 主族元素原子的电子层数等于其所在周期的周期序数 | |
| C. | 四、五、六周期中都含有18种元素,其中Ⅷ族中所含元素种类最多 | |
| D. | 元素周期表中有18列、16个族,且第二列中无非金属元素 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH3的电子式: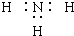 | |
| B. | 氯气的化学式:Cl | |
| C. | 氮气的电子式: | |
| D. | 硫酸铝的电离方程式:Al2(SO4)3═Al3++SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
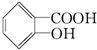 ,请回答下列问题:
,请回答下列问题: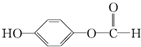 ;
; ,1mol该有机物在适宜条件下与氢氧化钠经过一系列反应,最多能消耗氢氧化钠的物质的量为(填序号)C;
,1mol该有机物在适宜条件下与氢氧化钠经过一系列反应,最多能消耗氢氧化钠的物质的量为(填序号)C;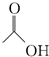 ,在一定条件下,水杨酸与乙酸酐可合成阿司匹林,阿司匹林可表示为:
,在一定条件下,水杨酸与乙酸酐可合成阿司匹林,阿司匹林可表示为: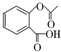 ,则阿司匹林的分子式为C9H8O4.
,则阿司匹林的分子式为C9H8O4.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.05 mol•L-1的H2SO4溶液pH=1 | |
| B. | 0.001 mol•L-1的NaOH溶液pH=11 | |
| C. | 0.005 mol•L-1的H2SO4溶液与0.01 mol•L-1的NaOH溶液等体积混合,混合溶液pH为6,溶液显酸性 | |
| D. | 完全中和pH=3的H2SO4溶液50 mL,需要pH=11的NaOH溶液50 mL |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com