
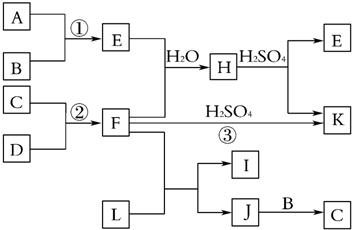
分析 由短周期元素的单质及其化合物的转化关系图可知,化合物E是形成酸雨的污染物之一,则E为SO2,A、B、C、D都是非金属单质,其中B、C、D在常温常压下是气体,则A为S,B为O2;化合物K是常用的氮肥,K为硫酸铵,所以F为氨气,则C、D分别为N2、H2;化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得,则L为NaClO,氨气与NaClO反应生成J,J由两种元素组成,它是火箭推进剂的成分之一,其相对分子质量为32,则J为N2H4;J与氧气反应生成C,C为氮气,再结合化学用语来解答.
解答 解:由短周期元素的单质及其化合物的转化关系图可知,化合物E是形成酸雨的污染物之一,则E为SO2,A、B、C、D都是非金属单质,其中B、C、D在常温常压下是气体,则A为S,B为O2;化合物K是常用的氮肥,K为硫酸铵,所以F为氨气,则C、D分别为N2、H2;化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得,则L为NaClO,氨气与NaClO反应生成J,J由两种元素组成,它是火箭推进剂的成分之一,其相对分子质量为32,则J为N2H4;J与氧气反应生成C,C为氮气,
(1)上述推断A为S,周期表中位置第三周期,第ⅥA族;
故答案为:第三周期,第ⅥA族;
(2)该反应为氨气与硫酸反应生成硫酸铵,化学反应为2NH3+H2SO4═(NH4)2SO4,
故答案为:2NH3+H2SO4═(NH4)2SO4;
(3)C为氮气,其结构式为N≡N,F为氨气,可以做致冷剂 制HNO3的原料等;
故答案为:N≡N; 做致冷剂、制HNO3等;
(4)L的溶液与化合物E反应,L为NaClO,E为SO2,在溶液中发生氧化还原反应生成氯化钠、硫酸钠,离子反应为ClO-+SO2+2OH-═Cl-+SO42-+H2O或ClO-+SO2+H2O═Cl-+SO42-+2H+,
故答案为:ClO-+SO2+2OH-═Cl-+SO42-+H2O或ClO-+SO2+H2O═Cl-+SO42-+2H+;
(4)由上述推断可知,J为N2H4,故答案为:N2H4.
点评 本题考查无机物的推断,利用物质的性质及转化关系图来推断出各物质是解答本题的关键,(3)中的离子反应为解答的易错点,注意结合氧化还原反应来解答,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:解答题
| MgO | AlO3 | MgCl2 | AlCl3 | |
| 熔点/℃ | 2852 | 2072 | 714 | 190(2.5×105Pa) |
| 沸点/℃ | 3600 | 2980 | 1412 | 182.7 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题


 ,②的反应类型为加成反应
,②的反应类型为加成反应
 (或
(或 )
)查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)某学生设计的用该浓盐酸与二氧化锰反应制取并收集干燥纯净的氯气的装置如图:
(1)某学生设计的用该浓盐酸与二氧化锰反应制取并收集干燥纯净的氯气的装置如图:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验编号 | KCIO3(g) | 催化剂 | 产生气体(mL) (已折算到标准情况) | 耗时(S) | ||
| 化学式 | 质量(g) | 回收 | ||||
| ① | 0.60 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
| ② | 0.60 | CuO | 0.20 | 90% | 67.2 | 79.5 |
| ③ | 0.60 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
| ④ | 0.60 | Cr2O3 | 0.20 | 异常 | 67.2 | 188.3 |
| 提出猜想 | 该刺激性气味的气体单质可能是Cl2 |
| 设计实验 验证猜想 | 实验步骤和结论(不要求写具体操作过程)将燃着的小木条插进集气瓶中,直至木条熄灭,用玻璃棒粘着湿润的碘化钾淀粉试纸插进集气瓶中.若试纸变蓝则证明是Cl2,否则不是氯气: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴乙烷中加入足量NaOH溶液加热,然后冷却,再加入AgNO3溶液有浅黄色沉淀生成 | |
| B. | 蔗糖溶液中加入稀H2SO4微热,再加少量新制Cu(OH)2浊液煮沸,有红色沉淀生成 | |
| C. | 将红色铜丝在酒精灯上加热后,立即插入无水乙醇中,铜丝恢复成原来的红色 | |
| D. | 用分液漏斗直接分离乙醇和苯的混合液 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com