
| A. | P3<P4,y轴表示A的转化率 | |
| B. | P3<P4,y轴表示B的体积分数 | |
| C. | P3<P4,y轴表示混合气体的密度 | |
| D. | P3>P4,y轴表示混合气体的平均摩尔质量 |
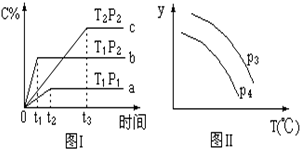
分析 根由图Ⅰ中a、b的相对位置知,先拐先平,压强大,增压(因p2>p1),C%升高,平衡正向进行故x=1;由b、c的相对位置知,先拐先平,温度高大,升温(因为T1>T2),C%降低.故正反应为放热反应,即该反应为:A(g)+B(g)?C(g)(正反应为放热反应),由反应式可知,升温和降压均可使反应向逆反应方向移动,据此结合图2答题.
解答 解:根由图Ⅰ中a、b的相对位置知,先拐先平,压强大,增压(因p2>p1),C%升高,平衡正向进行故x=1;由b、c的相对位置知,先拐先平,温度高大,升温(因为T1>T2),C%降低.故正反应为放热反应,即该反应为:A(g)+B(g)?C(g)(正反应为放热反应),由反应式可知,升温和降压均可使反应向逆反应方向移动
A、由于该反应是体积减小的反应,增加压强,平衡正向进行,A的转化率增大,则P3>P4,故A错误;
B、由于该反应正反应为放热反应,升高温度,平衡逆向进行,B的百分含量升高,图象不符合,故B错误;
C、由于该反应前后气体质量守恒,容器体积不变,所以密度一直不变,故C错误;
D、由于该反应是体积减小的反应,增加压强平衡正向移动,总物质的量减小,气体质量守恒,所以平均相对分子质量增大,则P3>P4,升高温度,平衡逆向移动,所以平均相对分子质量减小,图象符合,故D正确;
故选D.
点评 本题旨在考查学生对化学平衡图象的理解.解答这类图象题,首先要“译”出其化学含义.由于勒夏特列原理只适用于“单因素”(浓度或温度或压强)改变,分析时应固定一个物理量,分析另一物理量对纵坐标的影响,题目难度中等.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | Cl2通入NaOH溶液:Cl2+OH-═Cl-+ClO-+H2O | |
| B. | NaHCO3溶液中加入稀HCl:CO32-+2H+═CO2↑+H2O | |
| C. | 铁锈溶于过量醋酸:Fe2O3+6H+═2Fe3++3H2O | |
| D. | Cu溶于稀HNO3:3Cu+8H++2NO3-═3Cu2++2NO↑+4H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定有CO32- | |
| B. | 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO42- | |
| C. | 加入硝酸酸化的硝酸钡溶液既无沉淀也无气体生成,再加硝酸银溶液立即出现白色沉淀,一定有Cl- | |
| D. | 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ca2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
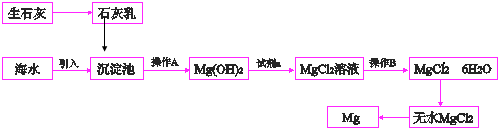
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
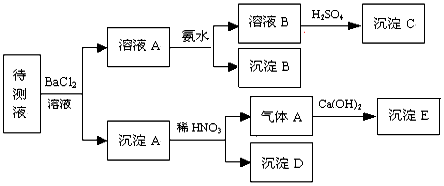
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 燃烧是将化学能只转化为热能 | |
| B. | 浓硫酸溶于水发热,所以该反应为放热反应 | |
| C. | 反应物的总能量高于生成物的总能量是放热反应 | |
| D. | 吸热反应是断裂化学键吸收的总能量小于形成化学键放出的总能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
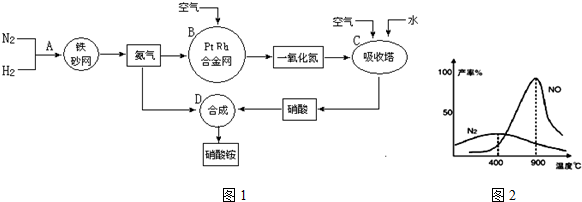
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ①②③④ | C. | ②③⑤⑥ | D. | ①②③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com