
 A、B、C、D、E、F六种物质的相互转化关系如图(反应件未标出),其中反应①是置换反应.
A、B、C、D、E、F六种物质的相互转化关系如图(反应件未标出),其中反应①是置换反应.
| ||
| ||
 ,反应③的化学方程式是4NH3+5 O2
,反应③的化学方程式是4NH3+5 O2
| ||
| △ |
 ;4NH3+5 O2
;4NH3+5 O2
| ||
| △ |


 数学奥赛暑假天天练南京大学出版社系列答案
数学奥赛暑假天天练南京大学出版社系列答案 南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案
南大教辅抢先起跑暑假衔接教程南京大学出版社系列答案科目:高中化学 来源: 题型:
| A、①③④ | B、①⑤ |
| C、②④⑤ | D、①②⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:

| 银氨溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
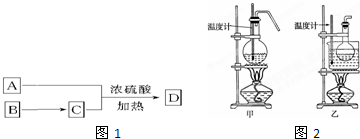
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、人工合成药物只有阿司匹林 |
| B、1853年,德国拜尔药厂的化学家霍夫曼合成了乙酰水杨酸 |
| C、青霉素是人工合成药物中的其中一种 |
| D、抗酸药除了含有碳酸氢钠、氢氧化铝和盐酸物质外,还含有调味剂和黏合剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
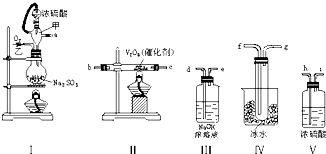
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
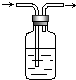 化学实验中的很多气体是用盐酸来制取的,这就导致了这些制取的气体中往往含有HCl杂质,要除去HCl杂质而得到纯净的目标气体,可用图所示装置.如果广口瓶中盛装的是饱和NaOH溶液,则可以用于下列哪种气体的除杂装置是(提示Cl2+H2O=HCl+HClO)( )
化学实验中的很多气体是用盐酸来制取的,这就导致了这些制取的气体中往往含有HCl杂质,要除去HCl杂质而得到纯净的目标气体,可用图所示装置.如果广口瓶中盛装的是饱和NaOH溶液,则可以用于下列哪种气体的除杂装置是(提示Cl2+H2O=HCl+HClO)( )| A、H2 |
| B、Cl2 |
| C、SO2 |
| D、CO2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com