
分析 (1)一般活泼非金属元素与活泼金属元素形成离子键,离子化合物中一定含有离子键,可能含有共价键;分子晶体中分子间以分子间作用力结合;
(2)离子晶体在熔融时破坏离子键;
(3)熔沸点的一般规律:原子晶体>离子晶体>分子晶体,结合物质常温下的状态分析.
解答 解:(1)一般活泼非金属元素与活泼金属元素形成离子键,离子化合物中一定含有离子键,可能含有共价键,NaCl中只含有离子键,NaHSO4中含有离子键和共价键;分子晶体中分子间以分子间作用力结合,干冰和碘片属于分子晶体,以分子间作用力结合;
故答案为:①④;①;⑤⑥;
(2)离子晶体在熔融时破坏离子键,NaHSO4属于离子晶体熔融状态下电离出钠离子和硫酸氢根离子,则电离方程式为:NaHSO4(熔融)=Na++HSO4-;
故答案为:离子键;NaHSO4(熔融)=Na++HSO4-;
(3)熔沸点的一般规律:原子晶体>离子晶体>分子晶体,①NaCl属于离子晶体,②金刚石属于原子晶体 ③Na属于金属晶体,常温下为固体,其熔沸点低于NaCl,⑤干冰属于分子晶体,常温下为气体,则熔沸点高低顺:②>①>③>⑤.
故答案为:②>①>③>⑤.
点评 本题考查了化学键、晶体的类型、熔沸点的比较,根据晶体的构成微粒及微粒间的作用力来分析解答,题目难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题

| A. | 甲装置工作时,正极发生发应为3AgO+6e-+3H2O=3Ag+6OH-; | |
| B. | 若乙装置选用阴离子交换膜时,则电解完成后,右侧溶液中含有FeO42-; | |
| C. | 每制得1mol Na2FeO4,理论上甲装置中消耗2mol NaOH; | |
| D. | 乙装置若选用阴离子交换膜,电解一段时间后,右侧溶液PH下降(忽略溶液体积改变). |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③ | B. | ①③④ | C. | ③④ | D. | ①②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 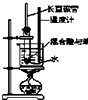 实验室制硝基苯 | B. |  石油分馏 | ||
| C. |  实验室用酒精制取乙烯 | D. | 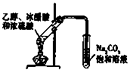 实验室制乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Na<Mg<Al | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 酸性强弱:H2SiO3<H2CO3<H2SO4 | D. | 原子最外层电子数:F>S>Ca |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
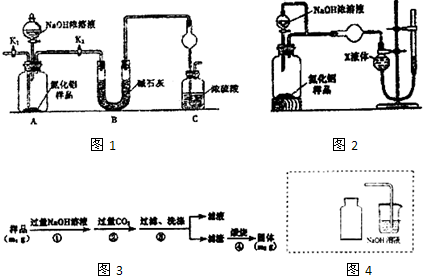

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 制备硝基苯,混合药品的顺序为:向试管中先加入苯,再加入浓硫酸,最后加入浓硝酸 | |
| B. | 银镜反应、乙醛与新制Cu(OH)2反应、实验室制取乙烯都必须用水浴加热 | |
| C. | 在重结晶的实验中,使用长颈漏斗趁热过滤是为了减少被提纯物质的损失 | |
| D. | 苯甲酸的重结晶实验中要得到纯净的苯甲酸固体需要进行至少两次过滤操作 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用铜和稀硫酸反应制取硫酸铜溶液 | |
| B. | 用石灰石除去氯化钙溶液中混有的盐酸 | |
| C. | 用氢氧化钠溶液除去二氧化碳中混有的氯化氢气体 | |
| D. | 用酚酞试液检验暴露在空气中的NaOH固体是否变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
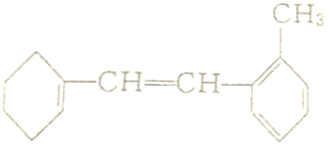
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com