
Ⅰ.如图所示,50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L,NaOH溶液在装置中进行中和反应.通过测定反应过程中所放出的热量,可计算中和热,回答下列问题:
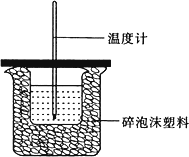
(1)图中装置缺少的仪器是________.
(2)下列说法中不正确的是________.(填字母,下同)
A.若用50 mL 0.55 mol·L-1的Ba(OH)2溶液代替NaOH溶液进行实验,测得的中和热是相同的
B.若用50 mL 0.50 mol·L-1的醋酸溶液代替盐酸进行实验,测得的中和热是相同的
C.若分别用等浓度的硫酸和Ba(OH)2溶液代替盐酸和NaOH溶液进行实验,测得的中和热是相同的
D.NaOH溶液稍过量的原因是让盐酸完全反应
Ⅱ.某学生用0.1 mol·L-1的盐酸标准溶液滴定未知浓度的20.00 mL氨水,用酚酞做指示剂,回答下列问题:
(1)在滴定时,左手握________(填仪器名称)的活塞,右手摇动锥形瓶,眼睛注视________.直到最后加入一滴盐酸后,溶液出现________现象,说明达到滴定终点,记录数据,发现消耗盐酸25.00 mL.
(2)下列操作中可能使所测氨水溶液的浓度数值偏低的是________.
A.酸式滴定管未用标准盐酸润洗,就直接注入标准盐酸
B.滴定前盛放氨水的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)当盐酸与氨水恰好完全反应生成盐时,消耗的盐酸溶液体积V________(填“>”、“<”或“=”)25.00 mL.
科目:高中化学 来源: 题型:阅读理解
 镁、铝、铁及其化合物在生产和生活中有广泛的应用.
镁、铝、铁及其化合物在生产和生活中有广泛的应用.| 实验序号 | I | II | III |
| 加入钢样粉末的质量(g) | 2.812 | 5.624 | 8.436 |
| 生成气体的体积(L)(标准状况) | 1.120 | 2.240 | 2.800 |
| 0.12 |
| 28.12 |
| 0.12 |
| 28.12 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
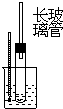 实验室制备少量硝基苯的主要步骤如下:
实验室制备少量硝基苯的主要步骤如下:查看答案和解析>>
科目:高中化学 来源: 题型:
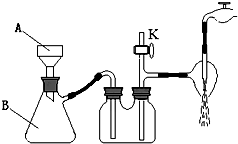 高氯酸钾广泛用于火箭及热电池业.实验室制取高氯酸钾的原理与苏教版《实验化学》中“硝酸钾晶体的制备”相同,步骤为:称取一定质量的KCl、NaClO4加热溶解,经冷却结晶、过滤、滤出晶体用蒸馏水多次洗涤及真空干燥得到.
高氯酸钾广泛用于火箭及热电池业.实验室制取高氯酸钾的原理与苏教版《实验化学》中“硝酸钾晶体的制备”相同,步骤为:称取一定质量的KCl、NaClO4加热溶解,经冷却结晶、过滤、滤出晶体用蒸馏水多次洗涤及真空干燥得到.| NaNO3 | KNO3 | NaCl | KCl | |
| 10°C | 80.5 | 20.9 | 35.7 | 31.0 |
| 100°C | 175 | 246 | 39.1 | 56.6 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com