
【题目】化合物丙由如下反应制得:
C4H10O![]() C4H8
C4H8 ![]() C4H8Br2(丙)
C4H8Br2(丙)
丙的结构简式不可能是
A. CH3CH2CHBrCH2Br B. CH3CH(CH2Br)2
C. CH3CHBrCHBrCH3 D. (CH3)2CBrCH2Br
科目:高中化学 来源: 题型:
【题目】下列根据实验操作和实验现象所得出的结论不正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 将FeCl2样品溶于盐酸后,滴加KSCN溶液 | 溶液变成红色 | 原FeCl2样品已变质 |
B | 将Na2SO3样品溶于水,滴加入稀盐酸酸化的Ba(NO3)2溶液 | 产生白色沉淀 | 原Na2SO3样品已变质 |
C | 向淀粉KI溶液中滴入3滴稀硫酸,再加入10%的H2O2溶液 | 滴入稀硫酸未见溶液变蓝;加入H2O2溶液后,溶液立即变蓝 | 酸性条件下,H2O2氧化性强于I2 |
D | 向5mL0.5mol/LNaHCO3溶液中滴入2mL1mol/LBaCl2溶液 | 产生白色沉淀,且有无色气体生成 | 反应的化学方程式为NaHCO3 + BaCl2 BaCO3↓+ NaCl+ CO2↑+H2O |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的数值,下列说法正确的是( )
A. 7.2 g CaO2晶体中阴离子和阳离子总数为0.3 NA
B. 0.1 mol/L NH4Cl溶液中Cl-离子数目为0.1 NA
C. 反应3H2(g)+N2(g)![]() 2NH3(g) ΔH=-92 kJ/mol,放出热量9.2 kJ时,转移电子0.6 NA
2NH3(g) ΔH=-92 kJ/mol,放出热量9.2 kJ时,转移电子0.6 NA
D. 0.1 mol H2O2分子中含极性共价键数目为0.3 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学想通过实验探究硫和碳得电子能力的强弱,通过比较它们最高价氧化物对应水化物的酸性强弱来验证,设计了如图实验。
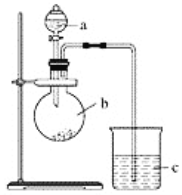
(1)仪器a的名称是________,应盛放下列药品中的________(填字母)。
A.稀硫酸 B.亚硫酸C.氢硫酸 D.盐酸
(2)仪器b的名称是________,应盛放下列药品中的________(填字母)。
A.碳酸钙 B.硫酸钠 C.氯化钠 D.碳酸钠
(3)仪器c中应盛放的试剂是________,如果看到的现象是____________________,证明b中反应产生了________,即可证明________比________酸性强,得电子能力________比________强,b中发生反应的离子方程式为______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I硼位于ⅢA族,三卤化硼是物质结构化学的研究热点,也是重要的化工原料。三氯化硼(BCl3)可用于制取乙硼烷(B2H6),也可作有机合成的催化剂。
查阅资料:①BCl3的沸点为12.5 ℃,熔点为-107.3 ℃;
②2B+6HCl![]() 2BCl3↑+3H2↑;
2BCl3↑+3H2↑;
③硼与铝的性质相似,也能与氢氧化钠溶液反应。
设计实验:某同学设计如图所示装置利用氯气和单质硼反应制备三氯化硼:

请回答下列问题:
(1)常温下,高锰酸钾固体粉末与浓盐酸发生的反应可替代A装置中的反应,而且不需要加热,两个反应的产物中锰的价态相同。写出高锰酸钾固体粉末与浓盐酸反应的离子方式:___________________ 。
(2)E装置的作用是_______________。如果拆去B装置,可能的后果是__________________________。
(3)三氯化硼遇水剧烈反应生成硼酸(H3BO3)和白雾,写出该反应的化学方程式:_________________;
(4)为了顺利完成实验,正确的操作是________(填序号).
①先点燃A处酒精灯,后点燃D处酒精灯
②先点燃D处酒精灯,后点燃A处酒精灯
③同时点燃A、D处酒精灯
(5)请你补充完整下面的简易实验,以验证制得的产品中是否含有硼粉:取少量样品于试管中,滴加浓_____________(填化学式)溶液,若有气泡产生,则样品中含有硼粉;若无气泡产生,则样品中无硼粉。
II.实验室现有3种酸碱指示剂,其pH的变色范围如下:甲基橙:3.1~4.4 石蕊:5.0~8.0 酚酞:8.2~10.0用0.1000 mol·L-1 NaOH溶液滴定未知浓度的CH3COOH溶液,反应恰好完全时,下列叙述正确的是 _____________________________
A.溶液呈中性,可选用甲基橙或酚酞作指示剂
B.溶液呈中性,只能选用石蕊作指示剂
C.溶液呈碱性,可选用甲基橙或酚酞作指示剂
D.溶液呈碱性,只能选用酚酞作指示剂
(6)使用酸碱中和滴定的方法,用0.01 moL/L盐酸滴定锥形瓶中未知浓度的NaOH溶液,下列操作能够使测定结果偏高的是___________________
A用量筒量取浓盐酸配制0.01 mol/L稀盐酸时,量筒用蒸馏水洗净后未经干燥直接量取浓盐酸
B配制稀盐酸定容时,俯视容量瓶刻度线
C滴定结束时,读数后发现滴定管下端尖嘴处悬挂有一滴液滴
D滴定过程中用少量蒸馏水将锥形瓶内壁附着的盐酸冲下
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下表中的电子、质子和中子的基本数据,讨论回答问题:
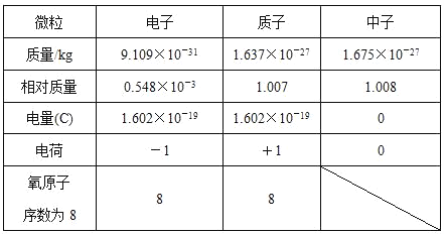
(1)决定原子质量的主要微粒是____________。
(2)原子相对质量的计算方法是_____________。
(3)如果1个质子和1个中子的相对质量都近似等于1,其原子的相对质量近似等于____________。
(4)原子中质子数、中子数、质量数之间的关系是_____。
(5)确定原子中质子数的方法是_________
(6)原子显电中性的原因是__________
(7)质子数为Z,质量数为A的X元素原子的组成符号是____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.用植物油可萃取溴水中的溴
B.苯酚具有弱酸性,俗称石炭酸
C.淀粉和纤维素互为同分异构体
D.可以用银镜反应检验淀粉是否水解完全
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表所列各组物质中,物质之间不能通过一步反应实现如图转化的是
A | B | C | D |
| |
甲 | Cu | Na2CO3 | Fe | NaAlO2 | |
乙 | CuO | NaOH | FeCl3 | Al2O3 | |
丙 | CuSO4 | NaHCO3 | FeCl2 | AlCl3 | |
丁 | Cu(NO3)2 | CO2 | Fe(NO3)2 | Al(OH)3 |
A. A B. B C. C D. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在恒压密闭容器中,充入一定量的H2和CO2 发生如下可逆反应:CO2(g)+3H2(g)![]() CH3OH(g)+H2O(g)ΔH <0,实验测得反应物在不同温度下,反应体系中CO2的平衡转化率与压强的关系曲线如图所示。
CH3OH(g)+H2O(g)ΔH <0,实验测得反应物在不同温度下,反应体系中CO2的平衡转化率与压强的关系曲线如图所示。

(1)该反应的ΔS______0(填>或<),该反应在_______(填“低温”或“高温”)条件下利于自发进行;
(2)比较T1与T2的大小关系:T1__T2(填“<”、“=”或“>”),理由是_______。
(3)在T1和P6的条件下,往密闭容器中充入3 mol H2和1 mol CO2,该反应在第5 min时达到平衡,此时容器的体积为1.8 L;则该反应在此温度下的平衡常数为____;若温度不变,压强恒定在P8的条件下重新达到平衡时,容器的体积变为_____L。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com