
| A. | CaCO3+2H+=Ca2++CO2↑+H2O | B. | 2Fe2++Cl2=2Fe3++2Cl- | ||
| C. | HCO3-+H+=CO2↑+H2O | D. | H++OH-=H2O |
分析 氧化还原反应的实质为电子转移、特征为化合价升降,所以氧化还原反应中一定存在元素化合价变化,据此对各选项进行判断.
解答 解:A、CaCO3+2H+=Ca2++CO2↑+H2O反应中不存在化合价变化,不属于氧化还原反应,故A错误;
B.2Fe2++Cl2=2Fe3++2Cl-,Cl、Fe元素的化合价发生变化,属于氧化还原反应,故B正确;
C.HCO3-+H+=CO2↑+H2O反应中不存在化合价变化,不属于氧化还原反应,故C错误;
D.H++OH-=H2O中,不存在化合价变化,不属于氧化还原反应,故D错误;
故选B.
点评 本题考查了氧化还原反应的判断,题目难度不大,明确氧化还原反应的实质、特征为解答关键,注意掌握四种基本反应类型与氧化还原反应之间的关系,试题有利于提高学生的灵活应用能力.


科目:高中化学 来源: 题型:实验题
| 实验次数 | 待测氢氧化钠溶液体积(mL) | 标准盐酸体积(mL) | NaOH溶液浓度(mol/L) | ||
| 初读数 | 末读数 | 体积 | |||
| 1 | 20.00 | 0.50 | 20.70 | 20.20 | 0.1059 |
| 2 | 20.00 | 6.00 | 26.00 | 20.00 | |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 45g水中含有的水分子数是2.5NA | |
| B. | 标准状况下,33.6LCO中含有的原子数是3NA | |
| C. | 0.5L、0.2mol/L的NaCl溶液中含有的Na+数是0.1NA | |
| D. | 1molCH4含电子数目为8NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 平均反应速度:乙>甲 | B. | 平衡时nc(甲)>nc(乙) | ||
| C. | 平衡时C的转化率:甲>乙 | D. | 平衡时A的物质的量甲>乙 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该溶液的PH=4 | |
| B. | 升高温度,溶液的PH增大 | |
| C. | 稀释时溶液中所有离子的浓度都减少 | |
| D. | 此酸的电离平衡常数约为1×10-9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 升高温度 | B. | 加入催化剂 | C. | .增大H2(g)的浓度 | D. | 增大NH3(g)的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3COO-、Cl-、NH4+、SO42- | B. | Mg2+、Cl-、Na+、NO3- | ||
| C. | K+、MnO4-、NO3-、Fe2+ | D. | Na+、SO42-、HCO3-、Cl- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
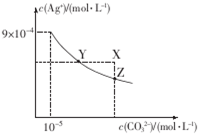 25℃时,已知AgCl的Ksp=1.8×10-10,Ag2CO3在水中的沉淀溶解平衡曲线如图所示,下列说法错误的是( )
25℃时,已知AgCl的Ksp=1.8×10-10,Ag2CO3在水中的沉淀溶解平衡曲线如图所示,下列说法错误的是( )| A. | Ag2CO3的Ksp为8.1×10-12 | |
| B. | Ag2CO3(s)+2Cl-(aq)?2AgCl(s)+CO32-(aq)平衡常数K=2.5×108 | |
| C. | 在Ag2CO3的饱和溶液中加入K2CO3(s)可使c(CO32-)增大(由Y点到Z点) | |
| D. | 在0.001mol•L-1AgNO3溶液中滴入同浓度的KCl和K2CO3的混合溶液,CO32-先沉淀 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com