
【题目】绿色化学提倡化工生产应提高原子利用率。原子利用率表示目标产物的质量与生成物总质量之比。在下列氮肥的制备反应中,原子利用率最高的是
A. NH3+H2O+CO2=NH4HCO3 B. 2NH3+CO2 ![]() CO(NH2)2+H2O
CO(NH2)2+H2O
C. 8NH3+3Cl2=N2+6NH4Cl D. 2NH3+2O2![]() NH4NO3+H2O
NH4NO3+H2O
科目:高中化学 来源: 题型:
【题目】Na2CO3俗名纯碱,下列对Na2CO3采用不同分类法的分类.不正确的是( )
A.Na2CO3是碱
B.Na2CO3是盐
C.Na2CO3是正盐
D.Na2CO3是钠盐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电镀污泥主要含有Cr2O3、NiO和Fe2O3等物质,可制备Na2Cr2O7溶液和NiSO4·6H2O晶体,实现有害物质的资源化利用。已知黄钠铁矾[NaFe3(SO4)2(OH)6]是一种浅黄色的难溶物,具有沉淀颗粒大、沉降速率快、容易过滤的特点。

(1)焙烧时Cr2O3被氧化为Na2CrO4,该反应的化学方程式为_______________。
(2)写出酸化时CrO42-转化为Cr2O72-的离子方程式:_________________。
(3)①加入CaCO3的目的是中和溶液中的酸,调节溶液pH,提高铁的去除率。溶液pH对除铁效率影响如下图所示。

则除铁时应控制溶液的pH为____________(填序号)。
A.0.5~1.5 B.1.5~2.5 C.2.5~3.5
②除铁时发生反应的离子方程式为___________。
③若除铁时pH稍大会生成Fe(OH)3胶体,显著降低除铁效率,原因是____________。
(4)从滤液中获取NiSO4·6H2O晶体的操作为________、冷却结晶、过滤、_________、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化铁可用作金属蚀刻、有机合成的催化剂,研究其制备及性质是一个重要的课题。
(1)氯化铁晶体的制备:
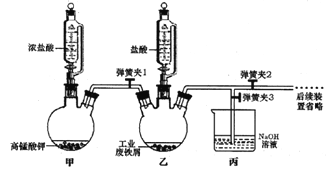
①实验过程中装置乙发生反应的离子方程式有________,仪器丙的作用为_________。
②为顺利达成实验目的,上述装置中弹簧夹打开和关闭的顺序为_______________。
③反应结束后,将乙中溶液边加入_____________,边进行加热浓缩、______、过滤、洗涤、干燥即得到产品。
(2)氯化铁的性质探究:
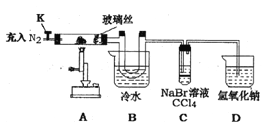
某兴趣小组将饱和FeC13溶液进行加热蒸发、蒸干灼烧,在试管底部得到固体。为进一步探究该固体的成分设计了如下实验。(查阅文献知:①FeC13溶液浓度越大,水解程度越小 ②氯化铁的熔点为306℃、沸点为315℃ ,易升华,气态FeCl3会分解成FeCl2和Cl2③ FeC12熔点670℃)
操作步骤 | 实验现象 | 解释原因 |
打开K , 充入氮气 | D中有气泡产生 | ①充入N2的原因________ |
关闭K, 加热至600℃,充分灼烧固体 | B中出现棕黄色固体 | ②产生现象的原因__________ |
实验结束,振荡C静置 | ③___________ | ④________________(用相关的方程式说明) |
⑤结合以上实验和文献资料,该固体可以确定的成分有______________________。 | ||
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机高分子材料M其结构简式为![]() ,下图是由有机物A(分子式为C5H8O)和苯甲醛为原料生产该有机物的合成路线。
,下图是由有机物A(分子式为C5H8O)和苯甲醛为原料生产该有机物的合成路线。

已知:① A分子中有两种不同环境的氢原子
② CH3CH2CH=CH2 ![]() CH3CHBrCH=CH2
CH3CHBrCH=CH2
CH3CHO+ CH3CHO ![]()
![]()
请回答以下问题:
(1)A的结构简式为_____,B 的名称为_____,F中所含官能团的名称是______。
(2)①和③的反应类型分别是_______、______;反应② 的反应条件为_______。
(3)反应④的化学方程式为______________。
(4)有机物E有多种同分异构体,其中同时符合下列条件的同分异构体有_____________种。
① 属于芳香酯类 ② 其酸性水解产物遇FeC13 显紫色
(5)以l-丙醇和NBS为原料可以制备聚丙烯醇(![]() )。请设计合成路线(其他无机原料任选)并用如下方式表示:__________________
)。请设计合成路线(其他无机原料任选)并用如下方式表示:__________________
![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】试管中盛有少量白色固体,可能是铵盐,检验的方法是( )
A.加水,将湿润的红色石蕊试纸放在试管口
B.加氢氧化钠溶液,加热,滴入紫色石蕊试剂
C.加氢氧化钠溶液,加热,滴入酚酞试剂
D.加氢氧化钠溶液,加热,将湿润的红色石蕊试纸放在试管口
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)完全燃烧0.1 mol某烃,燃烧产物依次通过浓硫酸、浓碱液,实验结束后,称得浓硫酸增重9 g,浓碱液增重17.6 g。该烃的化学式________,并写出其所有可能的结构简式:___________________。
(2)两种气态烃以任意比例混合,在120℃时1L该混合烃与9L氧气混合,充分燃烧后恢复到原状态,所得气体仍为10L。则两气态烃的分子的组成要符合的条件是_________________。
(3)如图所示,将浸透了石蜡油(分子中含有17个碳原子以上的液态烷烃混合物)的矿渣棉放置在硬质试管的底部,试管中加入碎瓷片,给碎瓷片加强热,石蜡油蒸气通过碎瓷片表面,发生反应,可得到一定量的气体生成物,用该生成物进行如下实验:
①生成的气体通入酸性KMnO4溶液中,溶液褪色。
②生成的气体通入Br2的CCl4溶液中,溶液褪色。
③用排水法收集一试管气体,点燃,燃烧时火焰明亮,有黑烟产生(甲烷燃烧时火焰为淡蓝色,无烟)。
根据以上现象思考:
A.用其最简单的同系物为例,写出②的反应方程式:___________。
B.碎瓷片的作用是_________________________。
C.产生黑烟的原因是_______________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T1 K时,向容积为2 L的密闭容器中充入一定量的CO和H2O(g),发生反应:CO(g)+H2O(g) ![]() CO2(g)+H2(g),反应过程中测定的部分数据如表(表中t2>t1)所示,下列说法错误的是
CO2(g)+H2(g),反应过程中测定的部分数据如表(表中t2>t1)所示,下列说法错误的是
反应时间/min | n(CO)/mol | n(H2O)/mol |
0 | 2.00 | 3.00 |
t1 | 0.80 | |
t2 | 1.80 |
A.用H2表示反应在t1 min内的平均速率为v(H2)=![]() mol·L1·min1
mol·L1·min1
B.保持其他条件不变,t1时向容器中充入3.00 mol N2,达到平衡时,n(CO2)=1.20 mol
C.保持其他条件不变,在t2 min时向容器中再通入1.00 mol CO,与原平衡相比,达到新平衡时CO的转化率将增大
D.温度升至T2 K,上述反应的平衡常数为0.70,则正反应的ΔH<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关能量转换的说法正确的是 ( )
A.煤燃烧是化学能全部转化为热能的过程
B.化石燃料和植物燃料燃烧时放出的能量均来源于太阳能
C.动物体内葡萄糖被氧化成CO2是热能转变成化学能的过程
D.植物通过光合作用将CO2转化为葡萄糖是太阳能转变成热能的过程
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com