
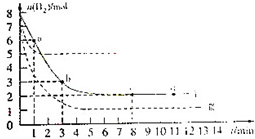
 ���Ź����ͼ۲����������ϳ�CH3OH������͵��о���Ϊ�ȵ㣮
���Ź����ͼ۲����������ϳ�CH3OH������͵��о���Ϊ�ȵ㣮| 6 |
| 3 |
| ||||
|
| 1 |
| 2 |
| 1 |
| 2 |


 �Ƹ�С״Ԫ�������������ϵ�д�
�Ƹ�С״Ԫ�������������ϵ�д� ����һ������ܼƻ�ϵ�д�
����һ������ܼƻ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
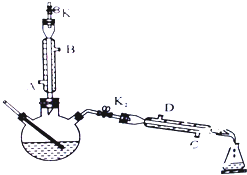 ��ͼ��ʾΪ��ȡ����������ʵ��װ�øĽ�ͼ����ش���������
��ͼ��ʾΪ��ȡ����������ʵ��װ�øĽ�ͼ����ش����������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
+ 4 |
2- 3 |
2- 4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
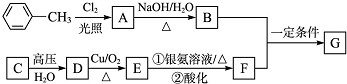
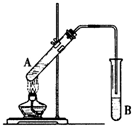 ���Թ�A�м���3mL�Ҵ���Ȼ����ܱ���������2mLŨ�����2mL���ᣬ����ͼ��ʾ���Ӻ�װ�ý���ʵ�飬����ȡ����������
���Թ�A�м���3mL�Ҵ���Ȼ����ܱ���������2mLŨ�����2mL���ᣬ����ͼ��ʾ���Ӻ�װ�ý���ʵ�飬����ȡ�����������鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��������Һ�е�c ��H+��=10-13mol/L |
| B��������Һ����ˮ���������c ��OH-��=10-13 mol/L |
| C�����ӵ��ռ���Һ��pH=13.0 |
| D��������Һ�е�c ��Mg2+��=5.6��10-10 mol/L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com