
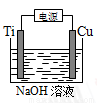
某小组设计电解饱和食盐水的装置如图,通电后两极均有气泡产生,下列叙述正确的是

A.铜是电解池的阳极
B.石墨电极附近溶液呈红色
C.铜电极上产生的是无色气体
D.石墨电极上发生还原反应
科目:高中化学 来源:2016-2017学年河北省邢台市高二上学期第四次月考化学卷(解析版) 题型:选择题
下列物质的电离方程式书写正确的是
A.NaHS==Na++H++S2- B.H2SO3 2H++SO32-
2H++SO32-
C.HClO==H++ClO- D.Fe(OH)3 Fe3++3OH-
Fe3++3OH-
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省肇庆市高二上学期期末化学试卷(解析版) 题型:填空题
(1)对于Ag2S(s)  2Ag+(aq)+ S2-(aq),其Ksp=____________(写表达式)。
2Ag+(aq)+ S2-(aq),其Ksp=____________(写表达式)。
(2)下列说法错误的是_______:
A.用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
B.多数物质的溶解度随温度的升高而增加,故物质的溶解都是吸热的;
C.对于Al(OH)3(s)  Al(OH)3(aq)
Al(OH)3(aq)  Al3++3OH-,前者为溶解平衡,后者为电离平衡;
Al3++3OH-,前者为溶解平衡,后者为电离平衡;
D.除去溶液中的Mg2+,用OH- 沉淀Mg2+ 比 用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3大;
用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3大;
E.沉淀反应中常加过量的沉淀剂,其目的是使沉淀完全。
(3)自然界原生铜的硫化物经氧化、淋滤作用后重生成CuSO4溶液,当这种溶液流向地壳深层遇到闪锌矿(ZnS)时,便会慢慢转化为铜蓝(CuS)[已知 Ksp(ZnS)=2.93×10-25、Ksp(CuS)=6.3×10-36],发生这种变化的原理是 。
(4)用右图装置,碱性条件下可以电解制备纳米Cu2O。反应为:2Cu+H2O Cu2O+H2↑,如下图所示。该电解池的阳极反应式为 。
Cu2O+H2↑,如下图所示。该电解池的阳极反应式为 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省肇庆市高二上学期期末化学试卷(解析版) 题型:选择题
已知:CO(g)+2H2(g) CH3OH(g) △H,反应过程中生成1mol CH3OH(g)的能量变化如 右下图所示。曲线Ⅰ、Ⅱ分别表示无或有催化剂两种情况。下列判断正确的是
CH3OH(g) △H,反应过程中生成1mol CH3OH(g)的能量变化如 右下图所示。曲线Ⅰ、Ⅱ分别表示无或有催化剂两种情况。下列判断正确的是
A.加入催化剂,△H变小
B.△H=+91 kJ/mol[
C.生成1molCH3OH(l)时,△H值增大
D.反应物的总能量大于生成物的总能量
查看答案和解析>>
科目:高中化学 来源:2017届吉林长春外国语学校高三上期末化学试卷(解析版) 题型:实验题
某氯化亚铁和氯化铁的混合物。现要测定其中铁元素的质量分数,按以下步骤进行实验:
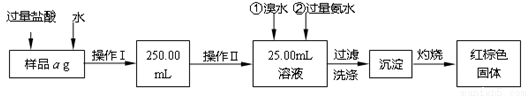
Ⅰ.请根据上面流程,回答以下问题:
(1)操作I所用到的玻璃仪器除烧杯、玻璃棒、250mL容量瓶外,还必须有 。(填仪器名称)
(2)溶解混合物时,加入盐酸的作用是 ;操作II中加入氯水的作用是 ;
(3)写出过量氨水参加反应的离子方程式 ;
(4)将沉淀物置于坩埚中灼烧至质量不再减少后冷却至室温,坩埚质量是b g,坩埚与加热后固体总质量是c g,则样品中铁元素的质量分数是 ;
Ⅱ.有同学提出,还可以采用以下方法来测定

(5)加过量还原剂可否用铁粉 ;
(6)若用酸性 KMnO4溶液滴定含Fe2+的溶液,写出反应的离子方程式 ;
查看答案和解析>>
科目:高中化学 来源:2017届吉林长春外国语学校高三上期末化学试卷(解析版) 题型:选择题
下列反应的离子方程式表示正确的是
A.用惰性电极电解NaCl溶液2H2O+2Cl- Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
B.铜片跟三氯化铁溶液反应:Fe3++Cu=Cu2++Fe2+
C.用FeSO4除去酸性废水中Cr2O72-:Cr2O72-+6Fe2++7H2O =2Cr3++6Fe3++14OH-
D.Fe3O4与稀HNO3反应:Fe3O4+8H+=Fe2++2Fe3++4H2O
查看答案和解析>>
科目:高中化学 来源:2017届湖北省高三1月质检化学试卷(解析版) 题型:填空题
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理。请回答下列问题:
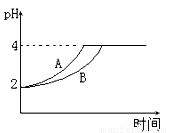
(1)常温下,取 pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如右图所示。则图中表示醋酸溶液中pH变化的曲线是 填“A”或“B”)。设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为 m2。 则 m1 m2 ( 选填“<”、“=”、“>”)。[来
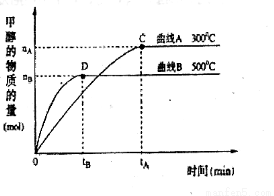
(2)在体积为3L的密闭容器中,CO与H2在一定条件下反应生成甲醇:CO(g)+2H2(g)  CH3OH(g)。升高温度,K值 (填“增大”、“减小”或“不变”)。在500℃,从反应开始到达到平衡,用氢气浓度变化表示的平均反应速率v(H2)= 。
CH3OH(g)。升高温度,K值 (填“增大”、“减小”或“不变”)。在500℃,从反应开始到达到平衡,用氢气浓度变化表示的平均反应速率v(H2)= 。
(3)某温度下Ksp[ Mg(OH)2] = 2×10 -11,若该温度下某MgSO4溶液里c(Mg 2+) =0.002 mol·L-1,如果生成Mg(OH)2沉淀,应调整溶液pH,使之大于 ;该温度 下,在0.20L的0.002mol/LMgSO4溶液中加入等体积的0.10mol/L的氨水溶液,该温度下电离常数Kb(NH3·H2O)=2×10-5,试计算 (填“有”或“无”) Mg(OH)2沉淀生成?
下,在0.20L的0.002mol/LMgSO4溶液中加入等体积的0.10mol/L的氨水溶液,该温度下电离常数Kb(NH3·H2O)=2×10-5,试计算 (填“有”或“无”) Mg(OH)2沉淀生成?
(4)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色。在分 析该溶液遇酚酞呈红色原因时,
析该溶液遇酚酞呈红色原因时, 甲同学认为是配制溶液所用的纯碱样品中混有NaOH 所致;乙同学认为是溶液中Na2CO3电离出的CO32-水解所致。
甲同学认为是配制溶液所用的纯碱样品中混有NaOH 所致;乙同学认为是溶液中Na2CO3电离出的CO32-水解所致。 请你设计一个
请你设计一个 简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论) 。
简单的实验方案给甲和乙两位同学的说法以评判(包括操作、现象和结论) 。
查看答案和解析>>
科目:高中化学 来源:2017届北京市丰台区高三上学期期末化学试卷(解析版) 题型:选择题
已知A(g)+B(g)  C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
温度/ ℃ | 700 | 800 | 830 | 1000 | 1200 |
平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
830℃时,向一个2 L的密闭容器中充入0.2mol的A和0.8mol的B,反应初始4 s内A的平均反应速率v(A)=0.005mol/(L·s)。下列说法正确的是
A.4 s时c(B)为0.38 mol/L
B.830℃达平衡时,A的转化率为20%
C.反应达平衡后,升高温度,平衡正向移动
D.1200℃时反应C(g)+D(g) A(g)+B(g)的平衡常数为0.4
A(g)+B(g)的平衡常数为0.4
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省长春市五县高二上期末化学试卷(解析版) 题型:选择题
工业废气H2S经资源化利用后可回收能量并得到单质硫。反应原理为:2H2S(g)+O2(g)=S2(s)+2H2O(l) △H=-632kJ·mol-1。H2S燃料电池的工作原理如图所示。下列说法不正确的是( )
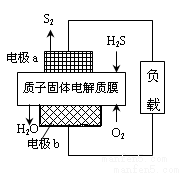
A.电极a为电池的负极
B.电极b上发生的电极反应为O2+4H++4e-=2H2O
C.若电路中通过2mol电子,则电池内部释放632kJ热能
D.若有17gH2S参与反应,则会有1molH+经质子膜进入正极区
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com