
【题目】某学习小组研究影响锌与稀硫酸反应速率的外界条件,设计实验的数据如下:
实验序号 | 锌的质量/g | 锌的状态 | c(H2SO4)/mol·L-1 | V(H2SO4)/mL | 反应前溶液的温度/℃ | 其他试剂 |
1 | 0.65 | 粒状 | 0.5 | 50 | 20 | 无 |
2 | 0.65 | 粉末 | 0.5 | 50 | 20 | 无 |
3 | 0.65 | 粒状 | 0.5 | 50 | 20 | 2滴CuSO4溶液 |
4 | 0.65 | 粉末 | 0.8 | 50 | 20 | 无 |
5 | 0.65 | 粉末 | 0.8 | 50 | 35 | 2滴CuSO4溶液 |
(1)在此5组实验中,判断锌和稀硫酸反应速率大小,最简单的方法可通过测定 进行判断,其速率最快的是 (填实验序号)。
(2)实验1和2表明 对反应速率有影响;实验1和3表明 对反应速率有影响。
(3)进行实验2时,小组同学根据实验过程绘制的氢气体积(标准状况下)与时间的关系如图所示。
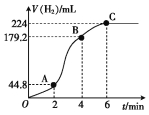
①在OA、AB、BC三段中反应速率最快的是 ,其原因是 。
②2~4 min内以硫酸的浓度变化表示的反应速率(假设溶液的体积不变)v(H2SO4)= mol·L-1·min-1。
【答案】(1)锌完全消失所需的时间;5
(2)固体反应物的表面积;(是否形成)原电池
(3)①AB;反应放热,使温度升高,反应速率加快②0.06
【解析】(1)判断锌和稀硫酸反应速率大小可通过测定锌完全消失所需的时间进行判断;5组实验数据进行对比不难看出,实验5用粉末状锌、更浓的硫酸、反应温度最高且滴加2滴CuSO4溶液,其反应速率最快。(2)对比实验1和2的实验条件可知,固体反应物的表面积对反应速率有影响;对比实验1和3的实验条件可知,原电池反应对反应速率有影响。(3)①OA、AB、BC三段反应时间相同,产生H2最多的一段反应速率最快;②2~4 min内产生H2的体积为179.2 mL-44.8 mL=134.4 mL,反应消耗的n(H2SO4)=n(H2)=0.006 mol,v(H2SO4)=0.06 mol·L-1·min-1。


科目:高中化学 来源: 题型:
【题目】(1)氯水具有多种性质,根据新制氯水分别与如图五种物质发生的反应填空(氯水足量):写出对应的化学方程式

① b ;
② c ;
③ e ;
(2)能证明氯水具有漂白性的现象是 ;
(3)久置的氯水变为 (填成份),用化学反应方程式表示为 。
(4)实验室还可用高锰酸钾快速地制取氯气,反应的化学方程式如下:
填写字母2KMnO4+16HCl(浓)=5Cl2↑+2MnCl2+2KCl+8H2O
①请用双线桥标出该反应的电子转移方向和数目 。
②该反应中的氧化剂是 ,若消耗0.2 mol氧化剂,则被氧化的还原剂的物质的量是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰化钠(化学式NaCN,C元素+2价,N元素-3价)是白色结晶颗粒、易潮解、剧毒、易溶于水、水溶液呈碱性。氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻污染。
(1)氰化钠溶液呈碱性,其原因是 (用离子方程式解释)。
(2)用双氧水处理NaCN产生一种酸式盐和一种能使湿润红色石蕊试纸变蓝的气体,写出该反应的化学方程式:________。
某化学兴趣小组在实验室制备硫代硫酸钠,并检测含氰化钠废水用硫代硫酸钠溶液处理后能否达标排放。
【实验一】实验室通过如下图所示装置制备Na2S2O3。

(3)装置a中盛装Na2 S03固体的仪器名称是 ,装置b的作用是________。
(4)装置c中的产物有Na2S2O3和CO2气体等,实验结束后,装置d中的溶质有NaOH、Na2CO3,还可能有 (填化学式)。
(5)实验结束后,在e处最好连接盛____(填“NaOH溶液”“水”或“CCl4”)的注射器,再关闭K2打开K1,防止拆除装置时污染空气。
【实验二】测定用硫代硫酸钠溶液处理后的废水中氰化钠的含量。已知:
①废水中氰化钠的最高排放标准为0.50 mg.L-l。
![]() ,AgI呈黄色,且CN-优先与Ag+反应,
,AgI呈黄色,且CN-优先与Ag+反应,
实验如下:取25.00 mL处理后的氰化钠废水于锥形瓶中并滴加几滴KI溶液作指示剂,用1.000×1 0-4mol.L-l的标准AgNO3溶液滴定,消耗AgNO3溶液的体积为2.50 mL。
(6)滴定终点的判断方法是________。
(7)处理后的废水中氰化钠的含量为 mg.L-l。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)将饱和FeCl3溶液滴入沸水中,煮沸一段时间后,当溶液变为红褐色时,停止加热,所得的分散系称为 ,该反应的化学方程式为 ;
(2)如果FeCl3溶液中含有少量的NaCl,要除去NaCl得到纯净的FeCl3溶液,有下列方案:

试剂①是 ;试剂②是 (均填化学式);“操作Ⅰ”为 (填操作名称)。加入试剂②后发生反应的离子方程式为 ;
(3)已知:2FeCl3+2KI=2FeCl2+I2+2KCl要从反应后的溶液中分离得到纯净的单质碘,需采取的操作有 、 、 (填操作名称)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.5L 1mol/L FeCl3溶液加水稀释至1L ,所得溶液中氯离子的物质的量浓度是( )
A.3mol/L B. 2mol/L C.1mol/L D. 1.5mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列物质的用途的说法错误的是
A.酚类化合物有毒,不能用于杀菌消毒
B.乙二醇可用于配制汽车防冻液
C.部分卤代烃可用作灭火剂
D.甲醛的水溶液(福尔马林)可用于防腐
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验小组研究可逆反应AsO43—+2I—+2H+![]() AsO33—+I2+H2O时,设计了如图所示的原电池:
AsO33—+I2+H2O时,设计了如图所示的原电池:

(1)电池工作时,盐桥中的阴离子向 极移动(填C1或C2);若向B池里滴加NaOH溶液,平衡向 方向移动,此时C2极的电极反应式为 。
(2)下列判断正确的是 。
a.微安表指针为0时,该反应处于平衡状态。
b.向A池中加入淀粉溶液,溶液变蓝说明该反应处于平衡状态。
c.AsO43—、AsO33—离子浓度相等时,该反应处于平衡状态。
(3)若在5min时间内电路中通过了1.204×104库伦电量,用I—浓度的变化来表示的化学反应速率为 。
(4)该反应的平衡常数表达式K= 。若升高温度,K值增大,则正反应的△H 0。(填“>”、“<”或“=”)
(5)已知反应达到平衡时,AsO43—离子转化率为25%,则I—离子的转化率 。
a.大于25% b.小于25%
c.等于25% d无法确定
(6)反应达到平衡后,若将AsO43—、I—、H+、AsO33—、I2的浓度均减少到原来的一半,上述平衡向 方向移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以Pt为电极,电解含有0.10molM+和0.10molN3+(M+、N3+均为金属阳离子)的溶液,阴极析出金属单质或气体的总物质的量(y)与导线中通过电子的物质的量(x)的关系如右图。对离子氧化能力的强弱判断正确的是(选项中H+为氢离子)

A. M+>H+>N3+
B. M+>N3+>H+
C. N3+>H+>M+
D. 条件不足,无法确定
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com