
 恒温恒容装置中发生如下反应:A(g)+2B(g)?2C(g)△H=-a kJ•mol-1(a>0),开始时充入一定量的A和B,B的反应速率随时间变化如图所示.下列说法正确是( )
恒温恒容装置中发生如下反应:A(g)+2B(g)?2C(g)△H=-a kJ•mol-1(a>0),开始时充入一定量的A和B,B的反应速率随时间变化如图所示.下列说法正确是( )| A. | 反应放出的热量一定小于a kJ | |
| B. | 5s后,反应停止,各物质浓度保持不变 | |
| C. | 5s末,ν(A):ν(B)=1:2 | |
| D. | 阴影部分面积可以表示A的物质的量浓度减少量 |
分析 A、参与反应的A、B的物质的量不知,所以无法求放出的热量的多少;
B、化学平衡是动态平衡;
C、只要反应发生,任一时刻速率之比对于对应物质的计量数之比;
D、纵坐标是B的速率,所以阴影部分面积可以表示B的物质的量浓度减少量.
解答 解:A、参与反应的A、B的物质的量不知,所以无法求放出的热量的多少,所以反应放出的热量不一定小于a kJ,故A错误;
B、化学平衡是动态平衡,5s后,各物质浓度保持不变,速率相等,但不为0,故B错误;
C、只要反应发生,任一时刻速率之比对于对应物质的计量数之比,所以5s末,ν(A):ν(B)=1:2,故C正确;
D、纵坐标是B的速率,所以阴影部分面积可以表示B的物质的量浓度减少量,而不是A的减少量,故D错误;
故选C.
点评 本题考查化学平衡的建立的过程,注意化学平衡是一种动态平衡,注重基础知识的考查,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | NaHCO3溶液与盐酸:CO32-+2 H+═H2O+CO2↑ | |
| B. | 向澄清的石灰水中加入过量的小苏打溶液:2HCO3-+Ca2++2OH-═CaCO3↓+2H2O+CO32- | |
| C. | 向硝酸亚铁溶液中加入稀硫酸:Fe2++4H++NO3-═Fe3++NO↑+2H2O | |
| D. | AlCl3溶液与过量氨水反应:Al3++4NH3•H2O═AlO2-+4NH4++2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | B. | CO2+C$\frac{\underline{\;\;△\;\;}}{\;}$2CO | ||
| C. | NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O↑+CO2↑ | D. | CaCO3+CO2+H2O═Ca(HCO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
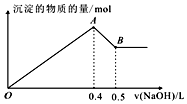 现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )
现有AlCl3和MgSO4混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如图所示,原溶液中Cl-与SO42-的物质的量之比为( )| A. | 1:3 | B. | 3:1 | C. | 2:3 | D. | 6:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:1:1 | B. | 2:1:1 | C. | 3:1:1 | D. | 1:2:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | SiO2是酸性氧化物不跟任何酸反应 | |
| B. | 水玻璃敞口存放,能有白色胶状沉淀析出 | |
| C. | 高温时SiO2能跟Na2CO3反应放出CO2,所以硅酸的酸性比碳酸强 | |
| D. | SiO2和CO2化学性质虽然相似,且两者的结构完全相同 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com