
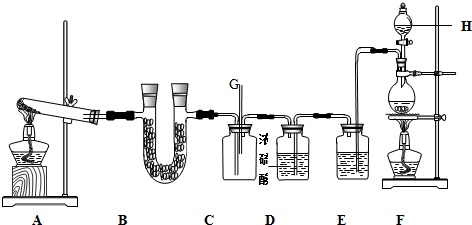
分析 由实验装置可知,A、F为为NH3和Cl2的发生装置,A中氨气与碱石灰可制取氨气,B中碱石灰干燥氨气,C为纯净、干燥的氯气与氨气反应的装置,发生8NH3+3Cl2═6NH4Cl+N2,F中发生MnO2+4HCl$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,E中饱和食盐水除去HCl,D中浓硫酸干燥氯气,以此来解答.
(1)装置F实验室用浓盐酸与二氧化锰在加热条件下制备氯气,反应生成氯化锰、氯气与水;
(2)稀盐酸还原性较弱,不能与二氧化锰发生氧化还原反应生成氯气;
(3)根据常见仪器的名称分析,E中用饱和食盐水除去HCl;
(4)氯气能够与氢氧化钠溶于反应,据此确定尾气处理的方法.
解答 解:(1)装置F用浓盐酸与二氧化锰在加热条件下制备氯气,反应生成氯化锰、氯气与水,反应离子方程式为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O,
故答案为:MnO2+4H++2Cl-$\frac{\underline{\;\;△\;\;}}{\;}$Mn2++Cl2↑+2H2O;
(2)根据方程式MnO2+4HCl(浓)$\frac{\underline{\;\;△\;\;}}{\;}$MnCl2+Cl2↑+2H2O,可知,
甲:HCl的物质的量为$\frac{146g}{36.5g/mol}$=4mol,但随着反应的进行,当为稀盐酸时反应停止,生成的氯气的物质的量小于1mol,
乙:MnO2的物质的量为$\frac{87g}{87g/mol}$=1mol,当1molMnO2完全反应时,生成1mol氯气,
所以乙生成氯气多,
故答案为:b;
(3)仪器H具有球形特征,且带有玻璃活塞,名称为分液漏斗,氯气在饱和食盐水中溶解度较小,氯化氢易溶于其中,所以装置E的作用是除去挥发出的氯化氢,
故答案为:分液漏斗;除去挥发出的氯化氢;
(4)黄绿色的有毒气体为氯气,氯气是酸性气体,能够与氢氧化钠反应生成氯化钠、次氯酸钠和水,所以可以用氢氧化钠来进行尾气处理,
故答案为:氢氧化钠.
点评 本题考查制备实验方案的设计,为高频考点,把握氯气的制备、氨气的制备及实验装置的作用为解答的关键,侧重分析与实验能力的综合考查,题目难度不大.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | ①④⑦⑧⑨ | B. | ②③⑤⑧⑩ | C. | ②④⑥⑧⑩ | D. | ①③④⑤⑦⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 化学式为C2H6O的化合物A具有如下性质:
化学式为C2H6O的化合物A具有如下性质:查看答案和解析>>
科目:高中化学 来源: 题型:实验题
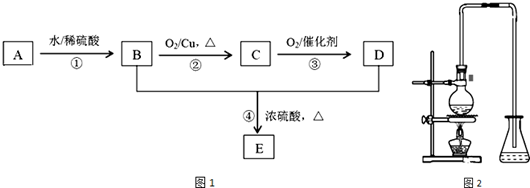
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气的热值高,无污染,是一种有待开发的“绿色能源” | |
| B. | 乙醇可以直接作为燃料,也可以和汽油混合作为发动机燃料 | |
| C. | 煤的气化和液化,即可以减少污染又可以提高燃烧的热效率 | |
| D. | 甲醇燃料电池不能得到推广应用,是由于能量转化率低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④ | B. | ②④ | C. | ①③ | D. | ①② |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
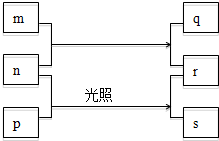 短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的化合物,且这几种化合物中每种都由2种元素组成.n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,r为一种一元强酸,s通常为难溶于水的混合物.上述物质的转化关系如图所示.
短周期元素W、X、Y、Z的原子序数依次增加.m、p、r是由这些元素组成的化合物,且这几种化合物中每种都由2种元素组成.n是元素Z的单质,通常为黄绿色气体,q的水溶液具有漂白性,r为一种一元强酸,s通常为难溶于水的混合物.上述物质的转化关系如图所示.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 具有相同结构式 | B. | 具有相同分子式 | ||
| C. | 具有不同相对分子质量 | D. | 具有不同原子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在由水电离出的c(OH-)=1×10-13mol/L的溶液中:Na+、Al3+、Cl-、NO3- | |
| B. | 在加入铝粉能产生H2的溶液中:NH4+、Fe2+、SO42-、NO3- | |
| C. | 在澄清透明的溶液中:Cu2+、K+、SO42-、Cl- | |
| D. | 在能使甲基橙变黄色的溶液中:Na+、CO32-、NO3-、K+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com