
| A. | 密度小于1.1g/mL的硝酸与金属反应,还原产物主要是NH4+ | |
| B. | 当硝酸溶液的密度为1.36g/mL时,Fe与过量硝酸反应的化学方程式为:4Fe+18HNO3=4Fe(NO3)3+3NO+3NO2+9H2O | |
| C. | 稀硝酸与金属反应,一定被还原成NO | |
| D. | 某硝酸试剂瓶的标签注明:密度1.26g/mL,质量分数50.0%;若取该试剂10mL配成1000mL溶液,所得溶液的物质的量浓度为1 mol/L |
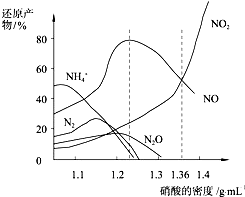
分析 A.密度小于1.1g•cm-3的硝酸与铁反应,还原产物百分率最多的是NH4+,最低的是二氧化氮;
B.当硝酸溶液的密度为1.36g•mL-1时,由图象可看出,生成的NO和NO2物质的量相等,反应的化学方程式应为4Fe+20HNO3=4Fe(NO3)3+3NO↑+3NO2↑+10H2O;
C.根据图片知,硝酸和Fe反应有多种含氮微粒生成;
D.该硝酸物质的量浓度=$\frac{1000ρω}{M}$mol/L=$\frac{1000×1.26×50%}{63}$=10mol/L,若取该试剂10ml配成100ml溶液,所得溶液物质的量浓度是1mol/L.
解答 解:A.根据图片知,密度小于1.1g•cm-3的硝酸与铁反应,还原产物百分率最多的是NH4+,最低的是二氧化氮,故A正确;
B.当硝酸溶液的密度为1.36g•mL-1时,由图象可看出,生成的NO和NO2物质的量相等,反应的化学方程式应为4Fe+20HNO3=4Fe(NO3)3+3NO↑+3NO2↑+10H2O,故B错误;
C.由图象可以看出,硝酸的浓度越大时,生成物的化合价越高,对应的硝酸的密度也越大,故C正确;
D.该硝酸物质的量浓度=$\frac{1000ρω}{M}$mol/L=$\frac{1000×1.26×50%}{63}$=10mol/L,若取该试剂10ml配成100ml溶液,所得溶液物质的量浓度是1mol/L,故D正确;
故选C.
点评 本题以硝酸为载体考查物质的量浓度计算、硝酸性质等知识点,正确获取图片信息是解本题关键,难点是D中质量分数与物质的量浓度之间的换算,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 84消毒液(主要成分NaClO)与洁厕剂混合使用可能会导致中毒 | |
| B. | 晶体硅可用于光伏发电、制造芯片,硅酸钠可用于制备硅胶和木材防火剂;硅胶可用作袋装食品的干燥剂 | |
| C. | 小苏打可中和胃酸、热纯碱可除去油污 | |
| D. | 二氧化硫可广泛用于食品的增白及漂白纸浆、毛、丝、草帽辫等 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若1mL PH=1盐酸与100mL MaOH溶液混合后,溶液PH=7,则NaOH溶液的PH=11 | |
| B. | 在滴有酚酞溶液的氨水中,加入NH4Cl的溶液恰好无色,则此时溶液的PH<7 | |
| C. | 某醋酸溶液的PH=a,将此溶液稀释1倍后,溶液的PH=b,则a>b | |
| D. | 1.0×10-3mol/L盐酸的PH=3.0,1.0×10-8mol/L盐酸PH=8.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. |  表示KNO3的溶解度曲线,a点所示的溶液是80℃时KNO3不饱和溶液 | |
| B. |  表示某放热反应分别在有、无催化剂的情况下反应过程中的能量变化 | |
| C. |  表示0.1000mol/LNaOH滴定20.00 mL 0.1000mol/L醋酸的滴定曲线 | |
| D. |  表示向NH4Al(SO4)2溶液中逐滴滴入Ba(OH)2溶液,体积V与沉淀n的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 人体内没有能使纤维素水解成葡萄糖的酶,因此纤维素不能作为人类的营养食物 | |
| B. | 严重影响我国北方的霾尘,其颗粒物是种胶体 | |
| C. | 大力实施矿物燃料“脱硫、脱硝技术”,可减少硫的氧化物和氮的氧化物对环境的污染 | |
| D. | 自来水厂常加入FeSO4和Cl2处理水,达到同时杀菌、消毒和聚沉水体中悬浮物的目的 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 20(2b-a) mol/L | B. | 20(b-2a) mol/L | C. | 10(2b-a) mol/L | D. | 10(b-2a) mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 剩余固体是铁、铜混合物 | |
| B. | 原固体混合物中铜的质量是6.4g | |
| C. | 反应后溶液中n(Fe3十)=0.l0mol | |
| D. | 反应后溶液中n(Fe2十)+n(Cu2十)=0.75mo1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com