
| ||
| m |
| M |
| ||
| ||
| m |
| M |
| 1.84��5��98% |
| 98 |
| ||
| 0.092 |
| 2 |



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ϩ�Ľṹ��ʽ��CH2CH2 |
| B���Ҵ����еĹ�������-OH����һ����λ����� |
C����������ģ��Ϊ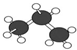 |
| D������ķ���ʽ��C2H4O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��CO2��SO2��CO�������������� |
| B���ƾ����ռ�����ᶼ�ǵ���� |
| C������ϡ�������Ȼ�����Һ���ǽ��� |
| D����ˮ��������Ư�۶��ǻ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
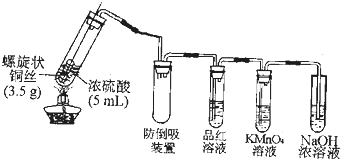
 CuCl��Ӧ�ù㷺���л��ϳɴ�����Ҳ��Ⱦ�Ϲ�ҵ������ʵЧ���������ռ������÷Ͼ�ӡˢ��·�����Ȼ���ͭ�ɼ�����Ⱦ��ʵ����Դ��������ش��������⣺
CuCl��Ӧ�ù㷺���л��ϳɴ�����Ҳ��Ⱦ�Ϲ�ҵ������ʵЧ���������ռ������÷Ͼ�ӡˢ��·�����Ȼ���ͭ�ɼ�����Ⱦ��ʵ����Դ��������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʵ�� ��� | KclO3��g�� | �������壨mL�� | ��ʱ ��s�� | |||
| ��ѧʽ | ������g�� | ʵ�ʻ��� | ||||
| 1 | 0.6 | - | - | - | 10 | 480 |
| 2 | 0.6 | MnO2 | 0.20 | 90% | 67.2 | 36.5 |
| 3 | 0.6 | CuO | 0.20 | 90% | 67.2 | 79.5 |
| 4 | 0.6 | Fe2O3 | 0.20 | 90% | 67.2 | 34.7 |
| 5 | 0.6 | Cr2O3 | 0.20 | �쳣 | 67.2 | 188.3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����ˮ���������c��H+��=10-12 mol?L-1����Һ�У�Cl-��CO32-��K+��SO32- |
| B�����д���AlO2-����Һ�У�K+��Al3+��Br-��HCO3- |
| C��ʹ���ȱ�����Һ�У�Fe2+��K+��NO3-��SO42- |
| D��ʹpH��ֽ������ɫ����Һ�У�Cl-��K+��Mg2+��SO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
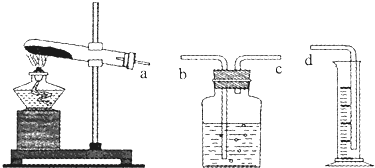
| A��������ͬ����ֱ�� |
| B�����ʺ��ɫ |
| C����������Ĥ |
| D�������ڲ����˶� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ﵽ��ѧƽ��״̬ʱ����c��CO��=0.100 mol?L-1����c��CO2��=0.0263 mol?L-1 |
| B����Ҫ���CO��ת���ʣ���Ӧ�ü����ʵ��Ĺ���FeO |
| C�������¶Ȼ�������ƽ����Է����������� |
| D��������56gFe�������յ�����С��a kJ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com