

���� ��1����ƽ��ʱ�μӷ�Ӧ������Ϊxmol����
PCl3��g��+Cl2��g��?PCl5��g��
��ʼ����mol����2 1 0
�仯����mol����x x x
ƽ������mol����2-x 1-x x
���º����£�ѹǿ֮�ȵ������ʵ���֮�ȣ��ݴ��з��̼���x���ٸ���v=$\frac{��c}{��t}$����v��Cl2����ƽ�ⳣ��K=$\frac{c��PC{l}_{5}��}{c��PC{l}_{3}����c��C{l}_{2}��}$��
��2��A������������������䣬�淴Ӧ���������ʵ�����С��ƽ����Է���������С�������淴Ӧ����ƽ����Է�������������
B������������������䣬�������ݻ����䣬�ܶ�ʼ�ղ��䣻
C���淴Ӧ���У�����Ӧ���ʼ��ͣ���Ӧ���ʲ��ٱ仯��˵������ƽ�⣻
D��t1ʱ�̺�PCl5��������������Cl2����������С��˵��t1ʱ��ʱ��Ӧ������Ӧ���У�
��3������Ũ����Qc����ƽ�ⳣ������ж�ƽ���Ƿ����ƶ����ƶ�������ƽ�ⲻ�ƶ��������ƶ���PCl3Ũ��һ����С����ƽ�������ƶ�����Ҫ���ƽ�ⳣ��������
��4����ƽ��ʱ��Ӧ��PCl5��g��Ϊymol����ʾ��ƽ��ʱ��������ʵ�����������ƽ�ⳣ������y��ֵ���ɣ�1���м����֪�ų�37.2kJ������ʱ�μӷ�Ӧ��������������ymolPCl5��g����Ӧ���յ�������
��5��̼���������������ᷴӦ�����Ȼ�����̼�����ƣ������ᡢ̼��ĵ���ƽ�ⳣ����֪������H3PO4��H2CO3��H2PO4-��HCO3-��HPO42-��̼���������������ᷴӦ����̼�����ơ�Na2HPO4��
��� �⣺��1����ƽ��ʱ�μӷ�Ӧ������Ϊxmol����
PCl3��g��+Cl2��g��?PCl5��g��
��ʼ����mol����2 1 0
�仯����mol����x x x
ƽ������mol����2-x 1-x x
���º����£�ѹǿ֮�ȵ������ʵ���֮�ȣ���$\frac{3-x}{3}$=$\frac{13}{15}$�����x=0.4��
��v��Cl2��=$\frac{\frac{0.4mol}{2L}}{5min}$=0.04mol/��L��min����ƽ�ⳣ��K=$\frac{c��PC{l}_{5}��}{c��PC{l}_{3}����c��C{l}_{2}��}$=$\frac{\frac{0.4}{2}}{\frac{2-0.4}{2}��\frac{1-0.4}{2}}$=$\frac{5}{6}$=0.83��
�ʴ�Ϊ��0.04��0.83��
��2��A������������������䣬�淴Ӧ���������ʵ�����С��ƽ����Է���������С�������淴Ӧ����ƽ����Է�������������ƽ����Է�����������˵������ƽ�⣬��A��ȷ��
B������������������䣬�������ݻ����䣬�ܶ�ʼ�ղ��䣬��B����
C���淴Ӧ���У�����Ӧ���ʼ��ͣ���Ӧ���ʲ��ٱ仯��˵������ƽ�⣬��C��ȷ��
D��t1ʱ�̺�PCl5��������������Cl2����������С��˵��t1ʱ��ʱ��Ӧ������Ӧ���У���D����
��ѡ��AC��
��3��ƽ�������������0.4molPCl3��0.2molCl2��0.2molPCl5��Ũ����Qc=$\frac{\frac{0.4-0.2}{2}}{\frac{1.6-0.4}{2}��\frac{0.6-0.2}{2}}$=0.83=K��ƽ�ⲻ�ƶ���c��PCl3����С��
�ʴ�Ϊ�����ƶ�����С��
��4����ƽ��ʱ��Ӧ��PCl5��g��Ϊymol����
PCl3��g��+Cl2��g��?PCl5��g��
��ʼ����mol����1 0 1
�仯����mol����y y y
ƽ������mol����1+y y 1-y
��$\frac{\frac{1-y}{2}}{\frac{1+y}{2}��\frac{y}{2}}$=$\frac{5}{6}$�����y=0.6��
�ɣ�1���м����֪0.4mol������Ӧ�ų�37.2kJ��������������0.6mol�������յ�����Ϊ37.2kJ��$\frac{0.6mol}{0.4mol}$=55.8kJ��
�ʴ�Ϊ��55.8kJ��
��5��̼���������������ᷴӦ�����Ȼ�����̼�����ƣ���Ӧ���ӷ���ʽΪ��H++CO32-=HCO3-�������ᡢ̼��ĵ���ƽ�ⳣ����֪������H3PO4��H2CO3��H2PO4-��HCO3-��HPO42-��̼���������������ᷴӦ����̼�����ơ�Na2HPO4����Ӧ���ӷ���ʽΪ��H3PO4+2CO32-=HPO42-+2HCO3-��
�ʴ�Ϊ��H++CO32-=HCO3-��H3PO4+2CO32-=HPO42-+2HCO3-��
���� ���⿼�黯ѧƽ����㡢��ѧƽ��״̬�жϡ�ƽ�ⳣ��������Ӧ�á�����ƽ�ⳣ��Ӧ�õȣ���3����Ũ���ж��в�����Ϊ���ʵ�����СŨ��һ����С������ƽ�ⳣ�������������״��㣬�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 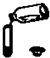 �㵹Һ�� | B�� |  �������� | C�� |  װ������ĩ | D�� |  Ϩ��ƾ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ����ij�¶�ʱ��n��N2����n��H2��=1��3�ı������������Ͷ���ܱ������з�Ӧ��N2��g��+3H2��g���T2NH3��g����H��0��
����ij�¶�ʱ��n��N2����n��H2��=1��3�ı������������Ͷ���ܱ������з�Ӧ��N2��g��+3H2��g���T2NH3��g����H��0���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��������һ����Ҫ�Ļ�����Ʒ��ijѧϰС����Ʒ����Ʊ������ᣮ��Ӧԭ�����£�
��������һ����Ҫ�Ļ�����Ʒ��ijѧϰС����Ʒ����Ʊ������ᣮ��Ӧԭ�����£� +2KMnO4$\stackrel{��}{��}$
+2KMnO4$\stackrel{��}{��}$ +KOH+2MnO2+H2O
+KOH+2MnO2+H2O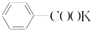 +HCl��
+HCl�� +KCl
+KCl
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������ʵĵ�����һ�����ȹ��̣��������������� | |
| B�� | ijЩ�����ˮ����һ�����ȹ��̣�����ˮ��̶����� | |
| C�� | ��Һ�������ȡ������Һ��������Ũ�ȵĴ�С | |
| D�� | ������Һ��һ��������Һ��������Һ��һ���Ǽ���Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ܷ���������Ӧ | |
| B�� | ��������������̼������������ͬ | |
| C�� | ������һ���������ܷ���ȡ����Ӧ | |
| D�� | �����������ǻ�Ϊͬ���칹�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com