
| A. | $\frac{36.5a}{22.4(a+1)d}$ | B. | $\frac{1000ad}{36.5a+22.4}$ | ||
| C. | $\frac{ad}{36.5a+22400}$ | D. | $\frac{1000ad}{36.5a+22400}$ |
分析 根据n=$\frac{V}{{V}_{m}}$计算出标准状况下aL氯化氢的物质的量,再根据m=nM计算出氯化氢的质量,从而得出所得溶液的质量,然后根据V=$\frac{m}{ρ}$计算出溶液体积,最后根据c=$\frac{n}{V}$计算出所得溶液的浓度.
解答 解:aL标准状况下的HCl的物质的量为:$\frac{aL}{22.4L/mol}$=$\frac{a}{22.4}$mol,质量为:36.5g/mol×$\frac{a}{22.4}$mol=$\frac{36.5a}{22.4}$g,
1L水的质量约为1000g,形成的溶液质量为:1000g+$\frac{36.5a}{22.4}$g,
该溶液的体积为:$\frac{1000g+\frac{36.5a}{22.4}g}{1000d/L}$=$\frac{22400+36.5a}{22400d}$L,
则所得溶液的物质的量浓度为:c(HCl)=$\frac{\frac{a}{22.4}mol}{\frac{22400+36.5a}{22400d}L}$=$\frac{1000ad}{22400+36.5a}$mol/L,
故选D.
点评 本题考查了物质的量浓度的计算,题目难度中等,正确计算所得溶液体积为解答关键,注意熟练掌握物质的量与气体摩尔体积、摩尔质量、物质的量浓度之间的关系,试题培养了学生的分析能力及化学计算能力.


科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 不慎碰翻燃着的酒精灯使酒精在桌面上燃烧起来,应立即用湿抺布灭火 | |
| B. | 不慎将酸沾到皮肤或衣物上,应立即用浓NaOH溶液清洗 | |
| C. | 用托盘天平称量物品质量时,物品应置于右盘 | |
| D. | 实验时应节约药品,实验剩余的药品应放回原试剂瓶 | |
| E. | 可燃性气体点燃前一定要验纯 | |
| F. | 可燃性气体点燃前一定要验纯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③ | B. | ②④ | C. | ①④ | D. | ②③ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

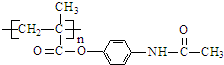 .
.

 与1mol O2恰好可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式
与1mol O2恰好可转化为1mol A和1mol B,且A与FeCl3溶液作用显紫色,写出A的稀溶液与过量浓溴水发生反应的化学方程式 .
. ;扑热息痛的结构简式为
;扑热息痛的结构简式为 .
. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com