
| ԭ������ | Ԫ�� | �й���Ϣ |
 | W | ��������Y��������������� |
| X | ��ͻ��ϼ�Ϊ-2 | |
| Y | ����Ԫ���ֽ��еĽ���Ԫ�� | |
| Z | ��Y��ԭ������֮��ΪW��Xԭ������֮�͵�3�� |
���� �������ڳ�ϡ�������������Ԫ��W��X��Y��Z��ԭ��������������X����ͻ��ϼ�Ϊ-2����XΪO��S��YΪ����Ԫ���ֽ��еĽ���Ԫ�أ���֪Xֻ��ΪO��YΪ�������ڵĽ���Ԫ�أ���Z��Y��ԭ������֮��ΪW��Xԭ������֮�͵�3������W��������Ϊx��Z��������Ϊz����10+x+z��=��x+8����3��z=14+2x��xֻ��Ϊ1����ZΪS�������⣬Ȼ����Ԫ�ػ�����֪ʶ�����
��� �⣺�������ڳ�ϡ�������������Ԫ��W��X��Y��Z��ԭ��������������X����ͻ��ϼ�Ϊ-2����XΪO��S��YΪ����Ԫ���ֽ��еĽ���Ԫ�أ���֪Xֻ��ΪO��YΪ�������ڵĽ���Ԫ�أ���Z��Y��ԭ������֮��ΪW��Xԭ������֮�͵�3������W��������Ϊx��Z��������Ϊz����10+x+z��=��x+8����3��z=14+2x��xֻ��Ϊ1����ZΪS�������⣬��WΪH��XΪO��YΪNa��ZΪS��
��1��XΪO��ZΪS���ʴ�Ϊ��O��S��
��2��X��Z������⻯��ˮ�������ֻ�����ۼ���S�ķǽ������������ȶ��Խ������⻯��ΪH2S���ʴ�Ϊ�����ۣ�H2S��
��3��NaOH�к����Ӽ���O-H���ۼ���Ϊ���ӻ�����ʴ�Ϊ�����ӣ����ۣ����ӣ�
��4����W��X��Y��Z����Ԫ����ɵij���������ΪNaHSO4��NaHSO3���������ʷ�����Ӧ�����ӷ���ʽΪH++HSO3-=SO2��+H2O���ʴ�Ϊ��NaHSO4��NaHSO3��H++HSO3-=SO2��+H2O��
���� ���⿼��λ�ýṹ�����ʼ�Ԫ�����ڱ���Ԫ�������ɣ�Ϊ��Ƶ���㣬����Ԫ�ص��ƶ�Ϊ���Ĺؼ����漰��ѧ�������ӷ�Ӧ�ȣ��ۺ��Խ�ǿ��ע�ػ���֪ʶ�Ŀ��飬��Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
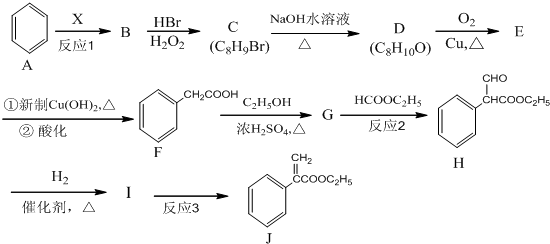
 ��G�Ľṹ��ʽΪ
��G�Ľṹ��ʽΪ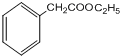 ��
��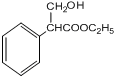

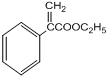 +H2O��
+H2O���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH4+��Al3+��NO3-��AlO2- | B�� | Na+��Fe3+��HSO3-��OH- | ||
| C�� | Cu2+��NH4+��SO42-��Cl- | D�� | K+��H+��I-��ClO- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���������pH������ʹ�����������NaOH��Һ��Ӧ������NaOH�����ʵ�����ͬ | |
| B�� | �����£�ij���ʵ�ˮ��Һ��pH��7���������һ�������ǿ�������� | |
| C�� | �����£�pH=12�İ�ˮ��pH=2������������ϣ�c��NH4+����c��Cl-����c��OH-����c��H+�� | |
| D�� | Na2CO3��Һ��ˮϡ�ͺָ���ԭ�¶ȣ�pH��KW����С |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ϩ�Ľṹ��ʽ��CH2CH2 | |
| B�� | ̼������ ���������������֮��ֵΪ3��2 ���������������֮��ֵΪ3��2 | |
| C�� | ˮ�������ӵĽṹʽΪ 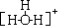 | |
| D�� | NaHCO3ˮ�ⷴӦ�����ӷ���ʽ��HCO3-+H2O?H3O++CO32- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
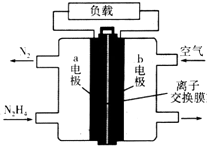 Һ��ȼ�ϵ�����������ȼ�ϵ�ؾ������С���ŵ㣮һ����Һ̬�£�N2H4��Ϊȼ�ϵĵ��װ����ͼ��ʾ���õ���ÿ����е�������Ϊ��������KOH��Һ��Ϊ�������Һ�����й��ڸõ�ص���������ȷ���ǣ�������
Һ��ȼ�ϵ�����������ȼ�ϵ�ؾ������С���ŵ㣮һ����Һ̬�£�N2H4��Ϊȼ�ϵĵ��װ����ͼ��ʾ���õ���ÿ����е�������Ϊ��������KOH��Һ��Ϊ�������Һ�����й��ڸõ�ص���������ȷ���ǣ�������| A�� | a���ķ�Ӧʽ��N2H4+4OH--4e-�TN2��+4H2O | |
| B�� | �ŵ�ʱ�����Ӵ�a��������������b�� | |
| C�� | �õ�س����ŵ�ʱ�����ӽ���Ĥ��ѡ�������ӽ���Ĥ | |
| D�� | ��·��ת�Ƶ���3NAʱ��������16.8 L |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��ͬ���칹��Ľṹ��ʽ��
��ͬ���칹��Ľṹ��ʽ�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͭ����ϡ�����У�3Cu+2NO3-+8H+=3Cu2++2NO��+4H2O | |
| B�� | ̼��������ᷴӦ��CO32-+2H+=H2O+CO2�� | |
| C�� | ����������Һ�м����������SO32-+2H+=SO2��+H2O | |
| D�� | ����ʯ���ڴ����У�CaCO3+2H+=Ca2++H2O+CO2�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com