
分析 (1)原溶液无色,KMnO4为紫红色,当溶液中的H2C2O4和KHC2O4反应完全时,溶液呈紫红色且半分钟颜色不变;
(2)步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,导致标准溶液氢氧化钠的体积增大,测定、KHC2O4的含量增大,草酸含量减小;
(3)令H2C2O4、KHC2O4的物质的量分别为xmol、ymol,根据①②中计算结果列方程计算,进而计算原样品中各自质量分数.
解答 解:(1)原溶液无色,而KMnO4为紫红色,所以当溶液中的H2C2O4和KHC2O4反应完全时,滴入最后一滴溶液呈紫红色且半分钟颜色不变;故答案为:溶液由无色变为浅红色(或紫色、紫红色),且半分钟内不褪色;
(2)步骤②中量取试样溶液时,酸式滴定管用蒸馏水洗过后没有润洗,导致标准溶液氢氧化钠的体积增大,测定、KHC2O4的含量增大,草酸含量减小,
故答案为:偏小;
(3)由于实验时所取溶液均为配置时的$\frac{1}{10}$,所以①、②中计算的数据均为配置溶液中溶质的$\frac{1}{10}$,由①得:2n(H2C2O4•2H2O)+n(KHC2O4)=0.05mol,由②得:n(H2C2O4•2H2O)+n(KHC2O4)=0.04mol,由上述两个方程式得:n(H2C2O4•2H2O)=0.01mol,n(KHC2O4)=0.03mol,故答案为:0.03mol.
点评 本题考查了氧化还原反应的计算及中和滴定的物质的量的计算,学生要注意250ml只取其中的$\frac{1}{10}$为易忽略的地方,难度中等.


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案 走进文言文系列答案
走进文言文系列答案科目:高中化学 来源: 题型:选择题
| A. | 沸点:F2<Cl2<Br2 | B. | 酸性:HClO4>H2SO4>H3PO4 | ||
| C. | 碱性:KOH>NaOH>Mg(OH)2 | D. | 离子半径:Na+>F->O2- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
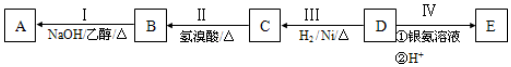
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
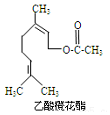 乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中正确的是( )
乙酸橙花酯是一种食用香料,其结构简式如图所示,关于该有机物的下列叙述中正确的是( )| A. | ①②③ | B. | ①②⑤ | C. | ①②⑤⑥ | D. | ①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10 | B. | 12 | C. | 24 | D. | 28 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 胆矾:CuSO4•5H2O | B. | 明矾:KAl(SO4)2•12H2O | ||
| C. | 石碱:Na2CO3•10H2O | D. | 绿矾:Fe2(SO4)3•7H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
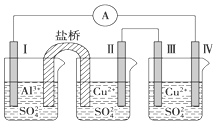 某同学组装了如图所示的电化学装置,电极Ⅰ为Al电极,其他均为Cu电极,则下列叙述正确的是( )
某同学组装了如图所示的电化学装置,电极Ⅰ为Al电极,其他均为Cu电极,则下列叙述正确的是( )| A. | 电流方向:电极Ⅰ→ →电极Ⅳ →电极Ⅳ | B. | 电极Ⅰ发生氧化反应 | ||
| C. | 电极Ⅱ质量不变 | D. | 电极Ⅲ的电极反应:2H++2e-═H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com