
 .
. 任意一种.
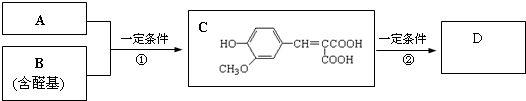
任意一种.分析 A对氢气的相对密度为52,则Mr(A)=52×2=104,1molA与足量NaHCO3溶液反应生成2mol气体,则A分子中含有2个-COOH.B属于芳香族化合物,且含有醛基,B与A反应生成C,由反应信息RCHO+CH2(COOH)$\stackrel{一定条件}{→}$RCH=C(COOH)2+H2O,结合C的结构可知,A为CH2(COOH)2,B为 ,C反应生成D,其分子式为C10H10O4,分子组成减少1分子CO2,由反应信息RCH=C(COOH)2$\stackrel{一定条件}{→}$RCH=CHCOOH+CO2↑可知,D的结构简式为
,C反应生成D,其分子式为C10H10O4,分子组成减少1分子CO2,由反应信息RCH=C(COOH)2$\stackrel{一定条件}{→}$RCH=CHCOOH+CO2↑可知,D的结构简式为 ,据此解答.
,据此解答.
解答 解:A对氢气的相对密度为52,则Mr(A)=52×2=104,1molA与足量NaHCO3溶液反应生成2mol气体,则A分子中含有2个-COOH.B属于芳香族化合物,且含有醛基,B与A反应生成C,由反应信息RCHO+CH2(COOH)$\stackrel{一定条件}{→}$RCH=C(COOH)2+H2O,结合C的结构可知,A为CH2(COOH)2,B为 ,C反应生成D,其分子式为C10H10O4,分子组成减少1分子CO2,由反应信息RCH=C(COOH)2$\stackrel{一定条件}{→}$RCH=CHCOOH+CO2↑可知,D的结构简式为
,C反应生成D,其分子式为C10H10O4,分子组成减少1分子CO2,由反应信息RCH=C(COOH)2$\stackrel{一定条件}{→}$RCH=CHCOOH+CO2↑可知,D的结构简式为 .
.
(1)C含有酚羟基、碳碳双键,可以发生氧化反应,含有羧基可以发生酯化反应,不能发生消去反应与水解反应,
故答案为:ad;
(2)由C的结构可知,1molC中含有2mol-COOH、1mol酚羟基-OH、1molC=C,
羧基、羟基与钠反应,1molC可以消耗3molNa,
羧基与碳酸氢钠反应,1molC消耗2molNaHCO3,
羧基、酚羟基与氢氧化钠反应,1molC消耗3molNaOH,
故等物质的量的C分别与足量的Na、NaHCO3、NaOH反应时消耗反应时消耗Na、NaHCO3、NaOH的物质的量之比为 3mol:2mol:3mol=3:2:3,
故答案为:3:2:3;
(3)由上述分析可知,A的结构简式为CH2(COOH)2,分子式为C3H4O4,D的结构简式为 ,含有的含氧官能团有:羧基、羟基、醚键,
,含有的含氧官能团有:羧基、羟基、醚键,
故答案为:C3H4O4;羧基、羟基、醚键;
(4)反应①的化学方程式是: ,
,
故答案为: ;
;
(5)D( )同分异构体符合:
)同分异构体符合:
①在苯环上只有两个取代基;
②在苯环上的一氯取代物只有两种,结合D的结构,说明两个不同的取代基处于对位位置或者两个相同的取代基处于邻位位置,
③1mol该同分异构体与足量NaHCO3反应生成2mol CO2气体,含有2个-COOH,
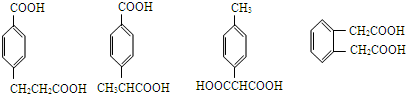
所以符合条件的D的同分异构体结构简式分别为: ,共有4种,
,共有4种,
故答案为:4; 任意一种.
任意一种.
点评 本题考查有机物的推断,涉及官能团的性质、同分异构体的书写,是对有机物知识的综合考查,利用题给信息,结合C的结构判断A、B的结构,能较好的考查学生的阅读、分析与思维能力,是有机热点题型,难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | R(OH)3 | B. | R2O7 | C. | HRO3 | D. | H2R |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 向2L的密闭容器中充入7.6mol NO和3.8mol O2,发生如下反应:
向2L的密闭容器中充入7.6mol NO和3.8mol O2,发生如下反应:| A. | 前5min反应的平均速率v(N2O4)=0.36mol•(L•min)-1 | |
| B. | T1℃时反应②的化学平衡常数K=0.6 | |
| C. | 反应①、②均为吸热反应 | |
| D. | 若起始时向该容器中充入3.6mol NO2和2.0mol N2O4,T1℃达到平衡时,N2O4的转化率为10% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 同种元素的原子均有相同的质子数和中子数 | |
| B. | 同主族元素的简单阴离子还原性越强,水解程度越大 | |
| C. | 同周期金属元素的化合价越高,其原子失电子能力越强 | |
| D. | 短周期第ⅣA与ⅦA族元素的原子间构成的分子,均满足原子最外层8电子结构 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答:
一定温度下,冰醋酸加水稀释过程中溶液的导电能力变化曲线如图所示,请回答:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com