
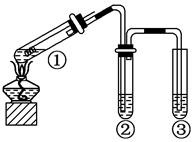
| A.上下移动①中铜丝可控制反应开始停止 |
| B.若②中是澄清石灰水,先浑浊后澄清 |
| C.③中KMnO4溶液褪色,说明SO2有还原性 |
D.①中反应离子方程式:Cu + 4 H+ + SO42-  Cu2+ + 2H2O + SO2↑ Cu2+ + 2H2O + SO2↑ |
科目:高中化学 来源:不详 题型:单选题
| A.通常情况下硫为浅黄色固体,而氯气为黄绿色的气体 |
| B.硫不溶于水而氯气溶于水 |
| C.跟金属或氢气反应时,硫被还原为-2价,而氯被还原为-1价 |
| D.跟Cu或Fe反应时,金属被硫氧化成低价态,而被氯氧化成高价态 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.CO2 | B.NH3 | C.C12 | D.HCl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 Fe2O3+SO2↑+ SO3↑+ 14H2O,将生成的气体通入BaCl2溶液中,下列叙述中正确的是
Fe2O3+SO2↑+ SO3↑+ 14H2O,将生成的气体通入BaCl2溶液中,下列叙述中正确的是| A.有BaSO4生成 | B.有BaSO3生成 |
| C.同时有BaSO4和BaSO3生成 | D.有SO3逸出 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com