
| A. | 1 mol石墨的总键能比1 mol金刚石的总键能小1.9 kJ | |
| B. | 石墨和金刚石的转化是物理变化 | |
| C. | 金刚石的稳定性强于石墨 | |
| D. | C(s、石墨)═C(s、金刚石)△H=+1.9 kJ•mol-1 |
分析 先根据图写出对应的热化学方程式,接着根据盖斯定律写出石墨转变成金刚石的热化学方程式,最后根据物质的能量越低越稳定来解答.
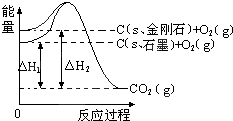
解答 解:由图得:①C(S,石墨)+O2(g)=CO2(g)△H=-393.5kJ•mol-1
②C(S,金刚石)+O2(g)=CO2(g)△H=-395.4kJ•mol-1,
利用盖斯定律将①-②可得:C(S,石墨)=C(S,金刚石)△H=+1.9kJ•mol-1,
A、由 C(S,石墨)=C(S,金刚石)△H=+1.9kJ•mol-1,1 mol石墨的总键能比1 mol金刚石的总键能大1.9 kJ,故A错误;
B、石墨和金刚石是不同的两种物质,石墨转化为金刚石属于化学变化,故B错误;
C、由C(S,石墨)=C(S,金刚石)△H=+1.9kJ•mol-1,金刚石能量大于石墨的总能量,物质的量能量越高越不稳定,则石墨比金刚石稳定,故C错误;
D、由 C(S,石墨)=C(S,金刚石)△H=+1.9kJ•mol-1,该反应的焓变为正值,故D正确.
故选:D.
点评 本题考查热化学方程式的书写及应用,题目难度不大,注意同素异形体之间的转化是化学反应和物质的能量越低越稳定.


 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案科目:高中化学 来源: 题型:解答题
 如图为Fe(OH)2制备实验的改进装置,使用该装置将能在较长时间内观察到白色絮状沉淀.请回答下列问题:
如图为Fe(OH)2制备实验的改进装置,使用该装置将能在较长时间内观察到白色絮状沉淀.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1种 | B. | 2种 | C. | 4种 | D. | 8种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 目前我国流通的硬币是由合金材料制造的 | |
| B. | 低碳钢、中碳钢和高碳钢中的碳含量依次降低 | |
| C. | 镁在空气中燃烧发出耀眼的白光,可用于制作照明弹 | |
| D. | 日用铝制品表面覆盖着氧化膜,对内部金属起保护作用 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D、E、F、G是原子序数依次增大的七种元素,其中A、B、C、D、E为短周期元素,F、G为第四周期元素.已知:A是原子半径最小的元素,B、C、D是紧邻的三个族的元素,C的三价阴离子和E的二价阳离子具有相同的电子层结构,F元素的基态原子具有六个成单电子,G是ⅠB族的元素.回答下列问题:
A、B、C、D、E、F、G是原子序数依次增大的七种元素,其中A、B、C、D、E为短周期元素,F、G为第四周期元素.已知:A是原子半径最小的元素,B、C、D是紧邻的三个族的元素,C的三价阴离子和E的二价阳离子具有相同的电子层结构,F元素的基态原子具有六个成单电子,G是ⅠB族的元素.回答下列问题: .B、C、D元素的第一电离能由大到小的顺序是N>O>C(用元素符号表示).
.B、C、D元素的第一电离能由大到小的顺序是N>O>C(用元素符号表示).查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯酚和苯甲醇互为同系物 | |
| B. | 塑料、合成纤维、涂料被称为“三大合成材料” | |
| C. | 天然油脂的主要成分是高级脂肪酸 | |
| D. | 淀粉和纤维素水解的最终产物都是葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氢气是一种理想的“绿色能源”,利用氢能需选择合适的储氢材料.目前正在研究和使用的储氢材料有镁系合金、稀土系合金等.
氢气是一种理想的“绿色能源”,利用氢能需选择合适的储氢材料.目前正在研究和使用的储氢材料有镁系合金、稀土系合金等. (g)$?_{高温}^{FeSO_{4}/Al_{2}O_{3}}$
(g)$?_{高温}^{FeSO_{4}/Al_{2}O_{3}}$ (g)+3H2(g)
(g)+3H2(g)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com