
用质量均为100g的Cu作电极,电解AgNO3溶液.稍电解一段时间后,两电极的质量相差28g,此时两电极的质量分别为( )
|
| A. | 阳极100 g,阴极128 g | B. | 阳极93.6 g,阴极121.6 g |
|
| C. | 阳极91.0 g,阴极119.0 g | D. | 阳极86.0 g,阴极114.0 g |
| 电解原理.. | |
| 分析: | 用铜作电极电解硝酸银溶液时,阳极上铜失电子发生氧化反应,电极反应式为Cu﹣2e﹣=Cu 2+,阴极上银离子得电子生成银,电极反应式为Ag++e﹣=Ag,电池反应式为Cu+2Ag+=2Ag+Cu 2+,两个电极质量差为溶解铜的质量和析出银的质量之和,根据转移电子相等计算两个电极的质量. |
| 解答: | 解:用铜作电极电解硝酸银溶液时,阳极上铜失电子发生氧化反应,电极反应式为Cu﹣2e﹣=Cu 2+,阴极上银离子得电子生成银,电极反应式为Ag++e﹣=Ag,电池反应式为Cu+2Ag+=2Ag+Cu 2+,设阴极析出银的质量为x,根据转移电子相等得阳极溶解铜的质量= 故选B. |
| 点评: | 本题以电解原理为载体考查物质的量的计算,正确理解“电解一段时间后两个电极质量差为溶解铜的质量和析出银的质量之和”为解答本题关键,再结合转移电子守恒解答即可,本题还可以采用排除法解答,阳极质量减少阴极质量增加,根据转移电子守恒知溶解铜的质量和析出银的质量不等,从而得出正确选项. |


科目:高中化学 来源: 题型:
下列有关溶液中微粒的物质的量浓度的关系,正确的是  ( )
( )
A.0.1 mol·L-1的NH4Cl溶液与0.05 mol·L-1的NaOH溶液等体积混合的溶液:
c(Cl-)>c(Na+)>c(NH )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
B.等物质的量的NaClO、NaHCO3混合溶液:c(HClO)+c(ClO-)=c(HCO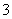 )+c(H2CO3)+c(CO
)+c(H2CO3)+c(CO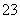 )
)
C.pH=2的HA溶液与pH=12的MOH溶液等体积混合:c(M+)=c(A-)>c(OH-)=c(H+)
D.某二元弱酸的酸式盐NaHA溶液:c(OH-)+c(H2A)=c(H+)+2c(A2-)
查看答案和解析>>
科目:高中化学 来源: 题型:
在酸性溶液中能大量共存,并且溶液为无色透明的是:
A. K+、Ca2+、HCO3-、Cl- B.Cu2+、Na+、NO3-、Cl-
C. Na+、K+、Mg2+、SO42- D.Mg2+、Fe3+、Cl-、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
已知以下两个氧化还原反应的化学方程式:
①Cl2+H2O===HCl+HClO
②2Al+Fe2O3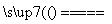 Al2O3+2Fe
Al2O3+2Fe
(1)用单线桥法表示反应②中的电子转移情况:______。
(2)若反应②中每生成1 mol Fe,转移电子的物质的量是:________。
(3)将反应①改写成离子方程式:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将c(H+)相同的盐酸和醋酸,分别用蒸馏水稀释至原来体积的m倍和n倍,稀释后两溶液的c(H+)仍相同,则m和n的关系是( )
|
| A. | m>n | B. | m<n | C. | m=n | D. | 不能确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氢氟酸在水溶液中建立如下电离平衡:HF⇌H++F﹣,如只改变一个条件一定可以使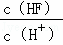 减小的是( )
减小的是( )
|
| A. | 通氯化氢气体 | B. | 加入少量氟化钾固体 |
|
| C. | 加入少氢氧化钠固体 | D. | 通入少量氟化氢气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
Li﹣SOCl2电池可用于心脏起搏器.该电池的电极材料分别为锂和碳,电解液是LiAlCl4﹣SOCl2.电池的总反应可表示为:4Li+2SOCl2=4LiCl+S+SO2.
(1)电池正极发生的电极反应为 ;
(2)SOCl2易挥发,实验室中常用NaOH溶液吸收SOCl2,有Na2SO3和NaCl生成. 如果把少量水滴到SOCl2中,实验现象是 ,反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
若NA表示阿伏加德罗常数,下列说法中,正确的是( )。
A.1 mol Cl2作为氧化剂得到的电子数为NA
B.在0 ℃,101 kPa时,22.4 L氢气中含有NA个氢原子
C.25 ℃,1.01×105 Pa,64 g SO2中含有的原子数为3 NA
D.NA个一氧化碳分子和0.5 mol甲烷的质量比为7∶4
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com