
| A£® | ³£ĪĀ³£Ń¹ĻĀ£¬46gNO2ŗ¬ÓŠ2NAøö·Ö×Ó | |
| B£® | ±ź×¼×“æöĻĀ£¬1.12L1H2ŗĶ0.2g2H2¾łŗ¬ÓŠ0.1NAøöÖŹ×Ó | |
| C£® | ŹŅĪĀŹ±£¬1LpH=2µÄNH4ClČÜŅŗÖŠĖ®µēĄė³öH+µÄŹżÄæĪŖ10-12NA | |
| D£® | ¹żŃõ»ÆĒā·Ö½āÖʵƱź×¼×“æöĻĀ1.12LO2£¬×ŖŅʵĵē×ÓŹżÄæĪŖ0.2NA |
·ÖĪö A”¢·Ö×ÓøöŹżN=$\frac{m}{M}{N}_{A}$£»
B”¢1H2ŗĶ2H2ÖŠÖŹ×ÓŹż¾łĪŖ2øö£»
C”¢NH4ClČÜŅŗÖŠ£¬ĒāĄė×ÓŗĶĒāŃõøł¾łĄ“×ŌÓŚĖ®µÄµēĄė£»
D”¢Ė«ŃõĖ®·Ö½āÖĘČ”ŃõĘų£¬ŃõŌŖĖŲµÄ¼ŪĢ¬ÓÉ-1¼Ū±äĪŖ0¼Ū£®
½ā“š ½ā£ŗA”¢·Ö×ÓøöŹżN=$\frac{m}{M}{N}_{A}$=$\frac{46g}{46g/mol}{N}_{A}$=NA£¬µ«ÓÉÓŚNO2ÖŠ“ęŌŚĘ½ŗā2NO2?N2O4£¬µ¼ÖĀ·Ö×ÓøöŹż¼õÉŁ£¬¹Ź·Ö×ÓŹżŠ”ÓŚNAøö£¬¹ŹA“ķĪó£»
B”¢±ź×¼×“æöĻĀ£¬1.12L1H2µÄĪļÖŹµÄĮæĪŖ0.05mol£¬¶ų0.2g2H2µÄĪļÖŹµÄĮæŅ²ĪŖ0.05mol£¬¶ų1H2ŗĶ2H2ÖŠÖŹ×ÓŹż¾łĪŖ2øö£¬¹Ź0.05mol1H2ŗĶ2H2¾łŗ¬0.1molÖŹ×Ó¼“0.1NAøö£¬¹ŹBÕżČ·£»
C”¢pH=2µÄNH4ClČÜŅŗÖŠ£¬ĒāĄė×ÓÅضČĪŖ0.01mol/L£¬ĒāŃõøłÅضČĪŖ10-12mol/L£¬ĒāĄė×ÓŗĶĒāŃõøł¾łĄ“×ŌÓŚĖ®µÄµēĄė£¬µ«ÓÉÓŚļ§øłĄė×ÓĖ®½ā½įŗĻĮĖ²æ·ÖĒāŃõøł£¬¹ŹČÜŅŗÖŠµÄĒāĄė×ÓŹĒĖ®µēĄė³öµÄČ«²æĒāĄė×Ó£¬¹ŹĖ®µēĄė³öµÄĒāĄė×ÓµÄĪļÖŹµÄĮæn=CV=0.01mol/L”Į1L=0.01mol£¬¼“0.01NAøö£¬¹ŹC“ķĪó£»
D”¢Ė«ŃõĖ®·Ö½āÖĘČ”ŃõĘų£¬ŃõŌŖĖŲµÄ¼ŪĢ¬ÓÉ-1¼Ū±äĪŖ0¼Ū£¬¹Źµ±Éś³É1molŃõĘųŹ±×ŖŅĘ2molµē×Ó¼“2NAøö£¬¹ŹD“ķĪó£®
¹ŹŃ”B£®
µćĘĄ ±¾Ģāæ¼²éĮĖ°¢·üŁ¤µĀĀŽ³£ŹżµÄÓŠ¹Ų¼ĘĖć£¬ŹģĮ·ÕĘĪÕ¹«Ź½µÄŹ¹ÓĆŗĶĪļÖŹµÄ½į¹¹ŹĒ½āĢā¹Ų¼ü£¬ÄŃ¶Č²»“ó£®


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| ČŻĘ÷ | ĪļÖŹ | ĘšŹ¼ÅضČ/£Ømol•L-1£© | Ę½ŗāÅضČ/£Ømol•L-1£© |
| ¢ń | N2O4 | 0.100 | 0.040 |
| NO2 | 0 | 0.120 | |
| ¢ņ | N2O4 | 0 | 0.014 |
| NO2 | 0.100 | 0.072 |
| A£® | Ę½ŗāŹ±£¬¢ń”¢¢ņÖŠ·“Ó¦ĪļµÄ×Ŗ»ÆĀŹ¦Į£ØN2O4£©£¼¦Į£ØNO2£© | |
| B£® | Ę½ŗāŹ±£¬¢ń”¢¢ņÖŠÉĻŹöÕż·“Ó¦µÄĘ½ŗā³£ŹżK£Ø¢ń£©=2K£Ø¢ņ£© | |
| C£® | Ę½ŗāŗó£¬ĻņĮ½ČŻĘ÷ÖŠ·Ö±šŌŁ³äČėŅ»¶ØĮæµÄNO2£¬£Ø¢ń£©ÖŠ$\frac{c£Ø{N}_{2}{O}_{4}£©}{c£ØN{O}_{2}£©}$µÄÖµ¼õŠ”£¬£Ø¢ņ£©$\frac{c£Ø{N}_{2}{O}_{4}£©}{c£ØN{O}_{2}£©}$ µÄÖµŌö“ó | |
| D£® | Ę½ŗāŗó£¬ÉżøßĪĀ¶Č£¬¢ń”¢¢ņÖŠĘųĢåŃÕÉ«¶¼½«±äÉī |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 1 | B£® | 2 | C£® | 3 | D£® | 4 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | Ńõ»ÆĪļ¶¼ŗ¬ÓŠŃõŌŖĖŲ£¬ĖłŅŌŗ¬ÓŠŃõŌŖĖŲµÄ»ÆŗĻĪļŅ»¶ØŹĒŃõ»ÆĪļ | |
| B£® | ĖįÓė¼ī·“Ӧɜ³ÉŃĪŗĶĖ®£¬ĖłŅŌÉś³ÉŃĪŗĶĖ®µÄ·“Ó¦Ņ»¶ØŹĒĖįŗĶ¼īµÄ·“Ó¦ | |
| C£® | Č¼ÉÕŅ»°ć¶¼°éĖę×Å·¢¹ā£¬·¢ČČĻÖĻó£¬ĖłŅŌÓŠ·¢¹ā£®·¢ČȵÄĻÖĻó¾ĶŹĒČ¼ÉÕ | |
| D£® | “¼ĄąĪļÖŹŌŚæÕĘųÖŠČ¼ÉÕÉś³ÉCO2 ŗĶH2O£¬¼×“¼ŹĒ“¼ĄąµÄŅ»ÖÖ£¬ĖłŅŌ¼×“¼ŌŚæÕĘųÖŠČ¼ÉÕÉś³ÉCO2 ŗĶH2O |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ś¢Ū | B£® | ¢Ū¢Ü | C£® | ¢Ł¢Ū | D£® | ¢Ł¢Ü |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
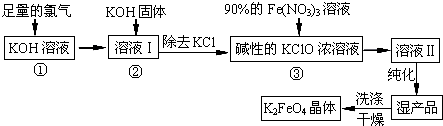
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | ¢Ü¢Ś¢Ż¢Ł¢Ū | B£® | ¢Ś¢Ü¢Ż¢Ł¢Ū | C£® | ¢Ü¢Ż¢Ś¢Ł¢Ū | D£® | ¢Ż¢Ś¢Ü¢Ł¢Ū |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
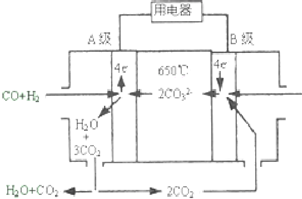 ČŪČŚĢ¼ĖįŃĪČ¼ĮĻµē³Ų£ØMCFS£©£¬·¢Ć÷ÓŚ1889Äź£®ĻÖÓŠŅ»øöĢ¼ĖįŃĪČ¼ĮĻµē³Ų£¬ŅŌŅ»¶Ø±ČĄżLi2CO3ŗĶNa2CO3µĶČŪ»ģŗĻĪļĪŖµē½āÖŹ£¬²Ł×÷ĪĀ¶ČĪŖ650”ę£¬ŌŚ“ĖĪĀ¶ČĻĀŅŌÄųĪŖ“߻ƼĮ£¬ŅŌĆŗĘų£ØCO”¢H2µÄĢå»ż±ČĪŖ1£ŗ1£©Ö±½Ó×÷Č¼ĮĻ£¬Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
ČŪČŚĢ¼ĖįŃĪČ¼ĮĻµē³Ų£ØMCFS£©£¬·¢Ć÷ÓŚ1889Äź£®ĻÖÓŠŅ»øöĢ¼ĖįŃĪČ¼ĮĻµē³Ų£¬ŅŌŅ»¶Ø±ČĄżLi2CO3ŗĶNa2CO3µĶČŪ»ģŗĻĪļĪŖµē½āÖŹ£¬²Ł×÷ĪĀ¶ČĪŖ650”ę£¬ŌŚ“ĖĪĀ¶ČĻĀŅŌÄųĪŖ“߻ƼĮ£¬ŅŌĆŗĘų£ØCO”¢H2µÄĢå»ż±ČĪŖ1£ŗ1£©Ö±½Ó×÷Č¼ĮĻ£¬Ę乤×÷ŌĄķČēĶ¼ĖłŹ¾£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com