
| 放电 |
| 充电 |
| A、放电时负极得电子,质量减轻 |
| B、放电时电解质溶液中的OH-向负极移动 |
| C、充电时阳极与外加电源的负极相连 |
| D、充电时阴极发生氧化反应 |


科目:高中化学 来源: 题型:
 已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH?CH3COO-+H+;△H>0
已知醋酸和盐酸是日常生活中极为常见的酸,在一定条件下,CH3COOH溶液中存在电离平衡:CH3COOH?CH3COO-+H+;△H>0| 测定次序 | 第一次 | 第二次 | 第三次 | 第四次 |
| V(mL) | 19.40 | 15.10 | 14.90 | 15.00 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Cu2++2OH-=Cu(OH)2↓ CuCO3+2NaOH=Cu(OH)2↓+Na2CO3 |
| B、CO32-+2H+=CO2↑+H2O BaCO3+2HCl=BaCl2+CO2↑+H2O |
| C、Ca2++CO32-=CaCO3↓ Ca(NO3)2+NaCO3=CaCO3↓+NaNO3 |
| D、H++OH-=H2O Ba(OH)2+2HNO3=Ba(NO3)2+2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、刚开始时两种溶液中产生H2的速率相同 |
| B、若有一种溶液中镁有剩余,则有剩余的是强酸溶液 |
| C、若两种溶液中镁均无剩余,则两者产生等量的氢气 |
| D、若两种溶液中镁均有剩余,则两者产生等量的氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
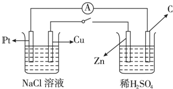 如图,将两烧杯用导线相连,Pt、Cu、Zn、C分别为四个电极,当闭合开关后,以下叙述正确的是( )
如图,将两烧杯用导线相连,Pt、Cu、Zn、C分别为四个电极,当闭合开关后,以下叙述正确的是( )| A、Cu极附近OH-浓度增大 |
| B、Cu极为原电池负极 |
| C、电子流向是由C极流向Pt极 |
| D、当C极上有4mol电子转移时,Pt极上有1mol O2生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 选项 | 实验操作 | 现象或原理 |
| A | 取少量KI溶液,先滴加氯水,再加入少量苯,振荡、静置 | 溶液分层,下层呈紫红色 |
| B | 将稀盐酸或氢氧化钠溶液慢慢滴入氢氧化铝胶体中 | 均先沉淀后溶解 |
| C | 将浓硝酸加入盛有铂、金的烧杯中,不反应,加入一定量浓盐酸后,铂、金溶解 | 浓盐酸氧化性强于浓硝酸 |
| D | 将40.0g NaOH固体溶于1.0L蒸馏水中配成溶液 | 溶液物质的量浓度为1.0mol?L-1 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 化学式 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | 1.8×l0-5 | 4.9×l0-10 | K1=4.3×l0-7, K2=5.6×l0-11 |
| A、NaCN+H2O+CO2(少量)=HCN+NaHCO3 |
| B、0.1mol?L-1的醋酸溶液中加入水或加入冰醋酸均可使平衡向电离方向移动 |
| C、等物质的量浓度的Na2CO3和NaCN溶液,后者溶液中水的电离程度大 |
| D、等pH的上述3种酸溶液,分别加水稀释后pH仍相等,则醋酸中加入水的体积最少 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向20mL0.5mol/LFeBr2(aq)中通入224mLCl2(标准状况):2Fe2++2Br-+2Cl2=2Fe3++Br2+4Cl- |
| B、在含有等物质的量的Fe(NO3)2和KI组成的混合溶液中滴入1~2滴盐酸:3Fe2++4H++NO3-=3Fe3++NO↑+2H2O |
| C、酸性条件下,用FeCl3溶液吸收水煤气中的H2S,以回收硫元素、降低污染:2Fe3++H2S=2Fe2++S↓+2H+ |
| D、Ca(ClO)2浓溶液中通入足量的SO2:ClO-+SO2+H2O=2H++Cl-+SO42- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com