
下列有关四个电化学装置的叙述正确的是
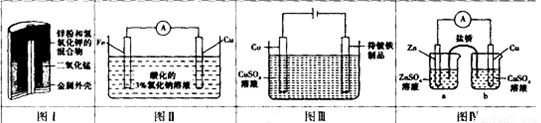
A.图I装置中MnO2作催化剂
B.图II装置工作一段时间后,滴加少量K3[Fe(CN)6]溶液,无明显现象
C.图III装置中Cu作阳极,为电解液提供Cu2+,保持溶液中Cu2+浓度恒定
D.图IV装置工作时,为平衡电荷,a烧杯中的Zn2+经盐桥移向b烧杯中
 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源:2013-2014山东省兰陵县下学期期中考试高二化学试卷(解析版) 题型:选择题
能够鉴定氯乙烷中氯元素的存在的操作是 ( )
A.在氯乙烷中直接加入AgNO3溶液
B.加蒸馏水,充分搅拌后,加入AgNO3溶液
C.加入NaOH溶液,加热后加入稀硝酸酸化,然后加入AgNO3溶液
D.加入NaOH的乙醇溶液,加热后加入AgNO3溶液
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省乳山市下学期期中考试高一化学试卷(解析版) 题型:选择题
下列四种X溶液,均能跟盐酸反应,其中反应最快的是
A.10℃ 20mL 3mol/L的X溶液 B.20℃ 30mL 2molL的X溶液
C.20℃ 10mL 4mol/L的X溶液 D.10℃ 10mL 2mol/L的X溶液
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省临沂市高三三模试卷理科综合化学试卷(解析版) 题型:选择题
常温下,相同pH的氢氧化钠和醋酸钠溶液加水稀释,平衡时pH随溶液体积变化的曲线如图所示,则
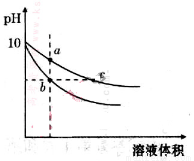
A.b、c两点溶液的导电能力相同
B.c点溶液中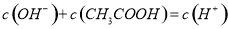
C.a、b、c三点溶液中水的电离程度a>c>b
D.用相同浓度的盐酸分别与等体积的b、c处溶液反应,消耗盐酸体积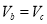
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省临沂市高三5月二模理综化学试卷(解析版) 题型:推断题
(12分)【化学——有机化学基础】
某有机化合物K的合成路线如下:‘
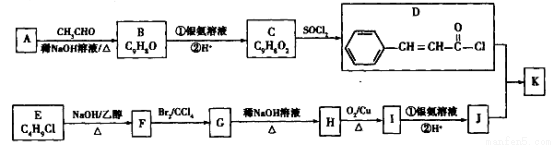
已知:
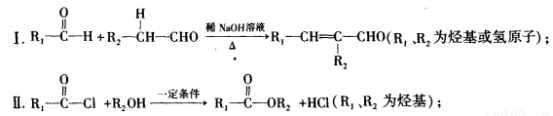
III.E的核磁共振氢谱图中只有一个吸收峰。
请回答下列问题:
(1)A的分子式为_______,C→D的反应类型为_______。
(2)鉴别E、G所用的试剂除NaOH溶液外,还需要的试剂有_______(填试剂名称)。
(3)符合下列条件的C的同分异构体共有_______种。
①能与溴水发生加成反应②能使氯化铁溶液显紫色
③苯环上有三个取代基且能发生银镜反应
(4)J在一定条件下可以发生聚合反应得到一种高聚物,该高聚物的结构简式为____ ____________________。
(5)D+J→K的化学方程式为________________________。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省临沂市高三5月二模理综化学试卷(解析版) 题型:选择题
X、Y、Z、W四种短周期元素的最外层电子数之和为24,它们在元素周期表中的位置如下图所示,下列说法一定正确的是
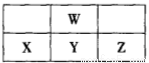
A.X、Y、Z的含氧酸的酸性依次增强
B.W元素形成的单核阴离子还原性强于X
C.W、X、Y的原子半径依次增大
D.W与氢元素形成的化合物中可能含有非极性键
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省下学期高二期末化学模拟试卷(解析版) 题型:选择题
某草药中有一种色素,它的结构简式为 ,用它制成的试剂可以检验物质的酸碱性。能够跟1 mol该化合物起反应的Br2(水溶液)或H2的最大用量分别是
,用它制成的试剂可以检验物质的酸碱性。能够跟1 mol该化合物起反应的Br2(水溶液)或H2的最大用量分别是
A. 3 mol、5 mol B. 6 mol、8 mol C. 10 mol、8 mol D. 6 mol、10 mol
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省东营市高三第二次模拟理科综合化学试卷(解析版) 题型:实验题
(18分)铵盐在工农业生产中有着重要的用途,请根据要求完成下列各题。
Ⅰ.某化学兴趣小组欲从下列装置中选取必要的装置制取(NH4)2SO4溶液。
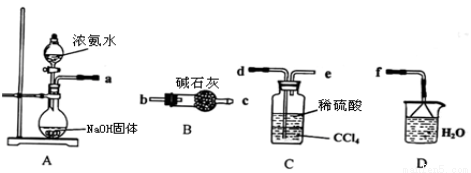
(1)仪器连接的顺序(用接口序号字母表示)是:a
(2)试从电离平衡角度分析该实验装置A中能产生氨气的原因:
。
(3)将装置C中两种液体分离开的操作名称是 。
(4)(NH4)2SO4“低毒,有刺激性,有吸湿性、吸湿后固结成块”。储存应注意 。
Ⅱ.为提高氯化铵的经济价值,我国化学家设计了利用氢氧化镁热分解氯化铵制氨气并得到碱式氯化镁[Mg(OH)Cl]的工艺。某同学根据该原理设计的实验装置如图:
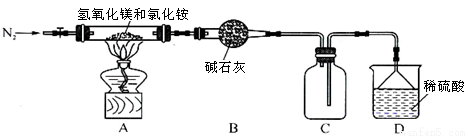
请回答下列问题:
(1)装置A中发生反应生成碱式氯化镁的化学方程式为 。
(2)反应过程中持续通入N2的作用有两点:一是使反应产生的氨气完全导出并被稀硫酸充分吸收,
二是 。
(3)由MgCl2溶液蒸发得到MgCl2·6H2O晶体,蒸发的目的是_________。
a.得到热饱和溶液 b.析出晶体
(4)镁是一种用途很广的金属材料,目前世界上60%的镁从海水中提取。
①若要验证所得无水MgCl2中不含NaCl,最简单的操作方法是:
。
②由MgCl2·6H2O制备无水MgCl2的操作在 氛围中进行,若在空气中加热,则会生成Mg(OH)Cl。
查看答案和解析>>
科目:高中化学 来源:2013-2014安徽省皖南八校高三第三次联考理综化学试卷(解析版) 题型:选择题
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.能与Cu反应产生气体的溶液:Na+、Fe2+、Cl-、 SO42-
B.滴入甲基橙显红色的溶液:K+、Cu2+、NO3-、I-
C.由水电离出的C (H+)·C(OH-)=10-24溶液:K+、Na+、NO3-、Cl-
D.无色溶液:K+、 Al3+ 、ClO-、SO42-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com