
| A. | 1:4 | B. | 10:11 | C. | 4:1 | D. | 5:22 |
 春雨教育同步作文系列答案
春雨教育同步作文系列答案科目:高中化学 来源: 题型:选择题
| A. | 食盐水、牛奶、豆浆 | B. | 碘酒、泥水、血液 | ||
| C. | 白糖水、食盐水、茶叶水 | D. | Ca(OH)2悬浊液、澄清石灰水、石灰浆 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
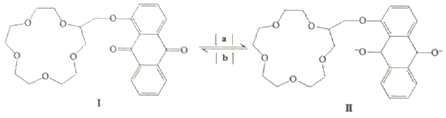
| A. | 物质Ⅰ的分子式是C25H28O8 | B. | 反应是氧化反应 | ||
| C. | 1molⅠ可与8molH2发生加成反应 | D. | 物质Ⅰ的所有原子不可能共平面 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Y与T形成的化合物中含有离子键 | |
| B. | X、Z、T对应的简单离子半径由大到小的顺序为T>X>Z | |
| C. | 1 mol Z的单质与足量X的单质反应,转移电子物质的量可能是2 mol,也可能是1 mol | |
| D. | X与Y形成的共价化合物XY2不能溶于强碱溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 与铁反应时分别生成硫化亚铁和氯化铁 | |
| B. | 与氢气反应的条件分别是加热和点燃(或光照) | |
| C. | 硫化氢的溶解度比氯化氢小得多 | |
| D. | 氯气能从氢硫酸中置换出单质硫 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com