
���� ��1��KspС���ȳ�������֪ͭ�����ȳ�����
��2�������ֳ�������ʱ��$\frac{c��B{r}^{-}��}{c��C{l}^{-}��}$=$\frac{Ksp��AgBr��}{Ksp��AgCl��}$��
��� �⣺��1������Ksp[Cu��OH��2]��Ksp[Mg��OH��2]������������Cu��OH��2���������������ӷ�ӦΪCu2++2NH3•H2O=Cu��OH��2��+2NH4+��
�ʴ�Ϊ��Cu��OH��2��Cu2++2NH3•H2O=Cu��OH��2��+2NH4+��
��2����ν�������棬����AgCl��AgBr���У�$\frac{c��B{r}^{-}��}{c��C{l}^{-}��}$=$\frac{Ksp��AgBr��}{Ksp��AgCl��}$=$\frac{5.4��1{0}^{-13}}{2.0��1{0}^{-10}}$=2.7��10-3���ʴ�Ϊ��2.7��10-3��
���� ���⿼�����ܵ���ʵ��ܽ�ƽ�⣬Ϊ��Ƶ���㣬����Ksp�ļ��㼰Ӧ��Ϊ���Ĺؼ������ط�������������Ŀ��飬��Ŀ�ѶȲ���


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
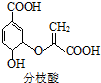
| A�� | �����к���3�ֺ��������� | |
| B�� | �ɷ���ȡ�����ӳɡ���ȥ���Ӿ۵ȷ�Ӧ | |
| C�� | �����ʵķ���ʽΪC10H10O6 | |
| D�� | 1mol��֦��������3molNaOH������Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| ���� | ���� | |
| A | ����NaOH��Һ | �к��ɫ���� |
| B | ����Ba��NO3��2��Һ | �а�ɫ���� |
| C | ��������KMnO4��Һ | ��ɫ��ȥ |
| D | ����K3[Fe��CN��6]�����軯�أ���Һ | ����ɫ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���д����ܷ�������������ȥ��Ӧ | |
| B�� | �ͼ������״����Ҵ����������Ҷ�����������ˮ������Ȼ��� | |
| C�� | ������ֱ�Ӻ��ǻ������Ļ�����һ���Ǵ� | |
| D�� | �Ҵ���Ũ���ᰴ1��3����Ȼ�ϡ����Ⱦ�һ��������ϩ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���·����ޡ��顢��˿�ijɷֶ�����ά�� | |
| B�� | �ع��͵���Ҫ�ɷ��Ǹ�֬������������������Ʒ��� | |
| C�� | ʯ�ͷ����Ŀ����Ϊ�˻����ϩ����ϩ��1��3-����ϡ | |
| D�� | �Ҵ�����������ͳ��������������������������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
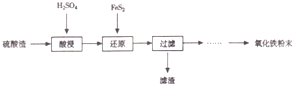
 �����Լ���������Һ�к���Fe3+�����������Fe3+�ɱ�������O2�����������ӷ�Ӧ����ʽ��ʾ��4Fe2++O2+4H+=4Fe3++2H2O
�����Լ���������Һ�к���Fe3+�����������Fe3+�ɱ�������O2�����������ӷ�Ӧ����ʽ��ʾ��4Fe2++O2+4H+=4Fe3++2H2O| ������ | Fe��OH��3 | A1��0H��3 | Fe��OH��2 | Mg��OH��2 | Mn��OH��2 |
| ��ʼ���� | 2.7 | 3.8 | 7.5 | 9.4 | 8.3 |
| ��ȫ���� | 3.2 | 5.2 | 9.7 | 12.4 | 9.8 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


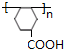 ��
��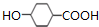 $��_{��}^{Ũ����}$
$��_{��}^{Ũ����}$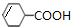 +H2O��
+H2O�� +4NaOH$��_{��}^{ˮ}$CH3CH2COONa+
+4NaOH$��_{��}^{ˮ}$CH3CH2COONa+ +2H2O+2NaCl��
+2H2O+2NaCl�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com