
分析 (1)依据题干中信息碳酸氢钠溶解度相对较小分析判断;
(2)①(I)依据用盐酸制取二氧化碳时常会含有氯化氢气体分析即可解答;
(II)依据稀硫酸能与氨气反应分析解答;
(Ⅲ)依据分离固体与液体采用的实验操作分析解答;
(3)依据化学方程式结合反应过程分析判断,依据生成沉淀为碳酸钙,加热碳酸氢钠分解后的混合物质量列方程计算.
解答 解:(1)a.碳酸氢钠易溶于水,故错误;
b.碳酸氢钠受热易分解,与其在溶液中首先结晶析出无关,故错误;
c.碳酸氢钠的溶解度相对于氯化铵来说碳酸氢钠的溶解度更小一些,所以在溶液中首先结晶析出,故正确;
d.碳酸氢钠的稳定性大于碳酸钠,与其在溶液中首先结晶析出无关,故错误;
故答案为:c;
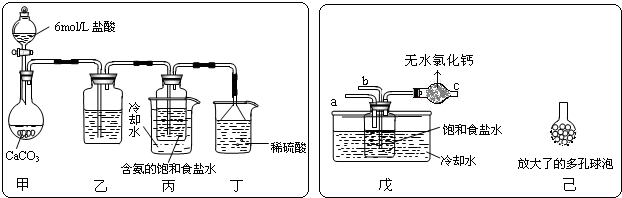
(2)(I)利用盐酸制取二氧化碳时,因盐酸易挥发,所以,二氧化碳中常会含有氯化氢气体,碳酸氢钠能与盐酸反应不与二氧化碳反应,所以通过碳酸氢钠的溶液是可以除掉二氧化碳气体中的氯化氢气体,
故答案为:饱和碳酸氢钠溶液;除去CO2中的HCl气体;
(II)实验过程中氨气可能有剩余,而稀硫酸能与氨气反应,所以稀硫酸的作用是吸收末反应的NH3,故答案为:吸收未反应的NH3;
(Ⅲ)分离出NaHCO3晶体的操作是分离固体与液体,常采用的实验操作是过滤操作,故答案为:过滤;
(3)碳酸氢钠受热发生的反应为:2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+CO2↑+H2O,与足量的石灰水充分反应,
NaHCO3+Ca(OH)2=CaCO3↓+H2O+NaOH;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
反应生成的碳酸钙物质的量为:$\frac{12g}{100g/mol}$=0.12mol;
设加热后的固体12.28g中含碳酸钠物质的量x、碳酸氢钠物质的量为y,依据题意得到:
①x+y=0.12、②106x+84y=12.28,
根据①②解得:x=0.1mol、y=0.02mol,
则所得固体中碳酸钠的质量分数为:$\frac{0.1mol×106g/mol}{12.28}$×100%=86.3%,
故答案为:86.3%.
点评 本题考查性质实验方案的设计,题目难度中等,是一道有关工业制纯碱知识的一道综合实验题目,考查学生分析和解决问题的能力,掌握制碱原理是解题的关键.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 | |
| B. | 不慎将浓碱沾到皮肤上,应立即用大量水冲洗,然后涂上硼酸溶液 | |
| C. | 稀释浓硫酸时,将浓硫酸沿器壁慢慢注入水中,并不断搅拌 | |
| D. | 实验室中酒精燃烧,小面积着火,立即用水扑灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
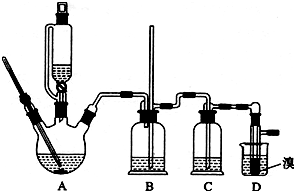
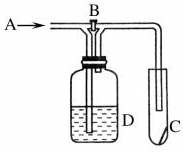 如图是一种试验某气体化学性质的实验装置,图中B为开关.若先打开B,在A处通入干燥的氯气,C中红色布条颜色无变化;当关闭B在A处通入干燥的氯气时,C中红色布条颜色褪去.则D瓶中盛有的溶液是( )
如图是一种试验某气体化学性质的实验装置,图中B为开关.若先打开B,在A处通入干燥的氯气,C中红色布条颜色无变化;当关闭B在A处通入干燥的氯气时,C中红色布条颜色褪去.则D瓶中盛有的溶液是( )| A. | 浓NaI溶液 | B. | 浓NaOH溶液 | C. | 饱和NaCl溶液 | D. | 浓硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
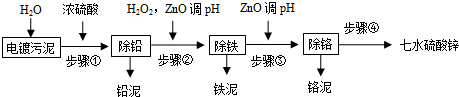
| 离子 | Fe2+ | Fe3+ | Cr3+ | Zn2+ |
| 开始沉淀的pH值 | 5.9 | 2.3 | 3.9 | 5.7 |
| 完全沉淀的pH值 | 8.3 | 3.2 | 5.6 | 8.3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm3 | 0.79 | 2.2 | 0.71 |
| 沸点/°C | 78.5 | 132 | 34.6 |
| 熔点/°C | -130 | 9 | -116 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
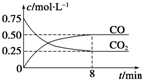 某温度下,在一密闭容器中充入一定量CO2,并加入足量铁粉,发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g),测得CO2和CO浓度随时间的变化如图所示:
某温度下,在一密闭容器中充入一定量CO2,并加入足量铁粉,发生反应:Fe(s)+CO2(g)?FeO(s)+CO(g),测得CO2和CO浓度随时间的变化如图所示:| 温度/K | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
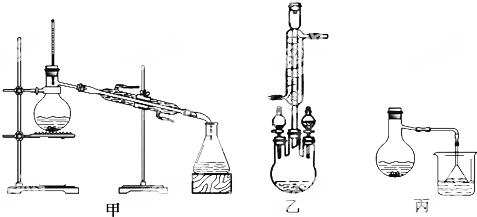
 )为原料,制取苯甲酸甲酯.已知有关物质的沸点如表:
)为原料,制取苯甲酸甲酯.已知有关物质的沸点如表:| 物质 | 甲醇 | 苯甲酸 | 苯甲酸甲酯 |
| 沸点/℃ | 64.7 | 249 | 199.6 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| T(℃) | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑤ | B. | ①②③⑤ | C. | ①②③ | D. | 全部 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com