
| A、1.2mol/(L?min) |
| B、1mol/(L?min) |
| C、0.6mol/(L?min) |
| D、0.4mol/(L?min) |
科目:高中化学 来源: 题型:
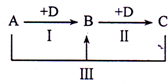 A、B、C、D表示中学化学中的四种常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去).
A、B、C、D表示中学化学中的四种常见物质,其中A、B、C均含有同一种元素,在一定条件下相互转化关系如图(部分反应中的水已略去).查看答案和解析>>
科目:高中化学 来源: 题型:
| A、该反应中的氧化剂只有Cu2O |
| B、氧化产物和还原产物的物质的量之比为1:6 |
| C、Cu既是氧化产物又是还原产物 |
| D、Cu2O在反应中既是氧化剂又是还原剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②④ | B、①③⑤ |
| C、②⑥ | D、②⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、平衡向正反应方向移动 |
| B、(a+b)>(c+d) |
| C、Z的体积分数变大 |
| D、X的转化率变小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、大力开发氢能源 |
| B、充分利用太阳能 |
| C、不使用含碳能源 |
| D、提高能源利用率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、正极为Fe,负极为Zn,电解质溶液为Fe2(SO4)3溶液 |
| B、阴极为Ag,阳极为Fe,电解质溶液为CuSO4溶液 |
| C、正极为Cu,负极为Fe,电解质溶液为CuSO4溶液 |
| D、正极为石墨,负极为Fe,电解质溶液为Fe2(SO4)3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaHCO3电离:NaHCO3=Na++H++CO32- |
| B、H3PO4电离:H3PO4?3H++PO43- |
| C、NH4+水解:NH4++H2O?NH3?H2O+H+ |
| D、CO32-水解:CO32-+H2O?H2CO3+2OH- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com