
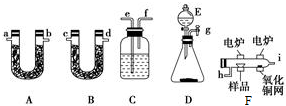
分析 (1)根据元素守恒法确定有机物的实验式确定所含元素;
(2)根据实验原理是测定一定质量的有机物完全燃烧时生成CO2和H2O的质量,来确定是否含氧及C、H、O的个数比,求出最简式.因此生成O2后必须除杂(主要是除H2O)明确各装置的作用是解题的前提,A用来吸收二氧化碳、B用来吸收水、C用于干燥通入E中的氧气、D用来制取反应所需的氧气、E是在电炉加热时用纯氧气氧化管内样品;根据一氧化碳能与氧化铜反应,可被氧化成二氧化碳的性质可知CuO的作用是把有机物不完全燃烧产生的CO转化为CO2;
(3)装置D是提供干燥氧气的装置,所以E中是液体,锥形瓶中为固体,混合反应生成氧气,试剂为过氧化氢和二氧化锰或过氧化钠和水等;
(4)CuO的作用是把有机物不完全燃烧产生的CO转化为CO2;
(5)经燃烧被吸收后A管质量增加1.76g为生成二氧化碳气体的质量,二氧化碳物质的量=$\frac{1.76g}{44g/mol}$=0.04mol,B管质量增加0.36g为水的质量,物质的量=$\frac{0.36g}{18g/mol}$=0.02mol,m(C)=0.04mol×12g/mol=0.48g,m(H)=0.02mol×2×1g/mol=0.04g,碳和氢元素质量=0.04g+0.48g=0.520g,则1.80g有机物样品中含有氧元素物质的量=$\frac{1.80g-0.52g}{16g/mol}$=0.08mol,据此计算有机物的实验式;
(6)题中该实验方法只能获得有机物的实验式,要确定有机物的分子式,还要知道有机物的相对分子质量或其摩尔质量;
(7)空气中二氧化碳、水影响有机物燃烧生成水、二氧化碳的质量,据此进行解答.
解答 解:(1)现准确称取1.80g有机物样品(含C、H元素,还可能含有O元素),经燃烧被吸收后A管质量增加1.76g为生成二氧化碳气体的质量,二氧化碳物质的量=$\frac{1.76g}{44g/mol}$=0.04mol,B管质量增加0.36g为水的质量,物质的量=$\frac{0.36g}{18g/mol}$=0.02mol,m(C)=0.04mol×12g/mol=0.48g,m(H)=0.02mol×2×1g/mol=0.04g,碳和氢元素质量=0.04g+0.48g=0.520g,则1.80g有机物样品中含有氧元素物质的量=$\frac{1.80g-0.52g}{16g/mol}$=0.08mol,此有机物的组成元素可能是C、H、O,
故答案为:C、H、O;
(2)D中生成的氧气中含有水蒸气,应先通过C中的浓硫酸干燥,在E中电炉加热时用纯氧氧化管内样品,生成二氧化碳和水,如有一氧化碳生成,则E中CuO可与CO进一步反应生成二氧化碳,然后分别通入B(吸收水)、A(吸收二氧化碳)中,根据产物的质量推断有机物的组成,则产生的氧气按从左到右流向,所选择装置各导管的连接顺序是gefhicd(或dc)ab(或ba),
故答案为:gefhicd(或dc)ab(或ba);
(3)装置D是提供干燥氧气的装置,所以E中是液体,锥形瓶中为固体,混合反应生成氧气,试剂为过氧化氢和二氧化锰或过氧化钠和水等,E和D中应分别装有药品H2O2和MnO2或H2O和Na2O2 ,
故答案为:H2O2和MnO2或H2O和Na2O2;
(4)CuO的作用是把有机物不完全燃烧产生的CO转化为CO2,若将CuO网去掉,A管增加的质量将减小,
故答案为:减小;
(5)称取1.80g有机物样品(含C、H元素,还可能含有O元素),经燃烧被吸收后A管质量增加1.76g为生成二氧化碳气体的质量,二氧化碳物质的量=$\frac{1.76g}{44g/mol}$=0.04mol,B管质量增加0.36g为水的质量,物质的量=$\frac{0.36g}{18g/mol}$=0.02mol,m(C)=0.04mol×12g/mol=0.48g,m(H)=0.02mol×2×1g/mol=0.04g,碳和氢元素质量=0.04g+0.48g=0.520g,则1.80g有机物样品中含有氧元素物质的量=$\frac{1.80g-0.52g}{16g/mol}$=0.08mol,n(C):n(H):n(O)=0.04:0.02×2:0.08=1:1:2,实验式为:CHO2,
故答案为:CHO2 ;
(6)由上述①可知该有机物的最简式为C2H4O,已经知道最简式,要确定有机物的分子式,则还要知道有机物的相对分子质量或样品的摩尔质量,所以B正确,
故答案为:B;
(7)由于装置内空气成分影响水、二氧化碳质量的测定,所以其目的是赶出装置内空气,减小实验误差,
故答案为:赶出装置内空气,减小实验误差.
点评 本题考查有机物组成的测定、物质性质实验方案的设计,题目难度中等,把握实验的原理和方法、明确实验操作目的是解答该题的关键,注意掌握质量守恒定律在确定有机物分子式中的应用,试题培养了学生的分析、理解能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
| A. | 纯碱常用于治疗胃酸过多 | |
| B. | 硫酸亚铁可用作缺铁性贫血的补血剂 | |
| C. | 用明矾进行自来水的杀菌消毒 | |
| D. | 碳酸钙不能用作人体补钙剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 液态氧、烧碱、碘酒 | B. | 白磷、生石灰、熟石灰 | ||
| C. | 铁、干冰、氯化氢 | D. | 氮气、空气、胆矾 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 微粒半径:Cl>S>N>O | B. | 稳定性:HF>HCl>HBr>HI | ||
| C. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | D. | 碱性:KOH>Ca(OH)2>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.
图是某化学兴趣小组探究不同条件下化学能转变为电能的装置.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 反应类型 | 反应条件 |
| A | 加成反应、取代反应、消去反应 | NaOH醇溶液/加热、NaOH水溶液/加热、常温 |
| B | 消去反应、加成反应、水解反应 | NaOH水溶液/加热、常温、NaOH醇溶液/加热 |
| C | 消去反应、加成反应、取代反应 | NaOH醇溶液/加热、常温、NaOH水溶液/加热 |
| D | 氧化反应、取代反应、消去反应 | 加热、NaOH醇溶液/加热、NaOH水溶液/加热 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com