
实验室测定含碘废液中I-的含量以及碘的回收过程如下:
Ⅰ.含碘废液中I-含量的测定
用移液管量取25.00 mL废液于250 mL锥形瓶中,分别加入5 mL 2 mol·L-1 H2SO4和10 mL 20% NH4Fe(SO4)2·12H2O溶液,摇匀。小火加热蒸发至碘完全升华,取下锥形瓶冷却后,加入10 mL 2 mol·L-1H2SO4,加入几滴二苯胺磺酸钠(用作指示剂),用0.0250 mol·L-1标准K2Cr2O7溶液进行滴定至终点。重复3次,数据记录如下表:
(已知反应:①2Fe3++2I-=2Fe2++I2 ②6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O)
次数 | 1 | 2 | 3 |
滴定体积(mL) | 19.60 | 19.65 | 19.55 |
Ⅱ.碘的回收
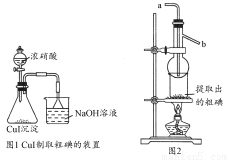
取250 mL含碘废液于烧杯中加入按上述计算所需的Na2S2O3溶液,并将CuSO4饱和溶液在不断搅拌下滴加到废液中,加热至70℃左右完全反应(已知:2I-+2Cu2++2S2O32-=2CuI↓+S4O62-)。过滤,得到的沉淀按图1进行操作。检查装置的气密性后,从分液漏斗中逐滴加入浓硝酸(注意滴液的速度)完全反应后,通过减压过滤,得到粗碘固体产品和抽滤液。然后按图2进行粗碘的提纯。
回答下列问题:
(1)用移液管量取废液时,将移液管竖直放入稍倾斜的锥形瓶中,接着的操作是______________________________________,数秒后,取出移液管。
(2)在盛有废液的锥形瓶中先加入5 mL 2 mol·L-1 H2SO4的目的是__________________________。
(3)根据滴定有关数据,该废液中I-含量是________g·L-1。
在滴定过程中,下列操作(其他操作正确)会造成测定结果偏低的是_____。
A.终点读数时俯视读数,滴定前平视读数
B.锥形瓶水洗后未干燥
C.滴定管未用标准K2Cr2O7溶液润洗
D.盛标准K2Cr2O7溶液的滴定管,滴定前有气泡,滴定后无气泡
(4)在图1锥形瓶中发生反应的化学方程式是____________________。
(5)按图2装置进行粗碘提纯,采用的分离方法是________,a、b为冷凝水进出口,其中________(选填a或b)接水龙头进水。最终得到较高纯度的单质碘。
(1)管尖与锥形瓶内壁接触,松开食指使溶液全部流出
(2)抑制Fe3+水解
(3)14.94(14.93~14.95均可给分) A
(4)2CuI+8HNO3=2Cu(NO3)2+4NO2↑+I2+4H2O
(5)升华法 a
【解析】(1)使用移液管时,应使管尖与锥形瓶内壁接触,然后松开食指使溶液全部流出。(2)加入稀硫酸是为了抑制Fe3+的水解。(3)由反应①、②可得出如下关系式:6I-~Cr2O72-,滴定消耗标准液K2Cr2O7溶液的体积V=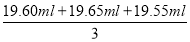 =19.60 mL,则:c(I-)×0.025 0 L=6×0.0250 mol·L-1×0.01960 L,解得c(I-)=0.1176 mol·L-1,则废液中I-的含量为0.1176mol·L-1×127 g·mol-1≈14.94 g·L-1。A项,滴定终点时俯视读数,滴定前平视读数,会造成标准液体积偏小而导致测定结果偏低;B项,对测定结果无影响;C项,标准液被稀释,造成滴定时所用体积偏大而使测定结果偏高;D项,标准液滴定前有气泡,滴定后无气泡,使标准液读取体积偏大,使测定结果偏高。故选A。(4)CuI中Cu+和I-均可被浓HNO3氧化,根据得失电子守恒、原子守恒可写出:2CuI+8HNO3=2Cu(NO3)2+4NO2↑+I2+4H2O。(5)图2是利用升华法提纯碘,冷凝水应从a口进,使碘蒸气更易凝结为固体碘。
=19.60 mL,则:c(I-)×0.025 0 L=6×0.0250 mol·L-1×0.01960 L,解得c(I-)=0.1176 mol·L-1,则废液中I-的含量为0.1176mol·L-1×127 g·mol-1≈14.94 g·L-1。A项,滴定终点时俯视读数,滴定前平视读数,会造成标准液体积偏小而导致测定结果偏低;B项,对测定结果无影响;C项,标准液被稀释,造成滴定时所用体积偏大而使测定结果偏高;D项,标准液滴定前有气泡,滴定后无气泡,使标准液读取体积偏大,使测定结果偏高。故选A。(4)CuI中Cu+和I-均可被浓HNO3氧化,根据得失电子守恒、原子守恒可写出:2CuI+8HNO3=2Cu(NO3)2+4NO2↑+I2+4H2O。(5)图2是利用升华法提纯碘,冷凝水应从a口进,使碘蒸气更易凝结为固体碘。


科目:高中化学 来源:2014高考化学苏教版总复习 专题7化学反应速率与化学平衡练习卷(解析版) 题型:选择题
在密闭的容器中进行如下反应:H2(g)+I2(g)  2HI(g),在温度T1和T2时,产物的量和时间的关系如图所示,根据图像判断正确的是( )
2HI(g),在温度T1和T2时,产物的量和时间的关系如图所示,根据图像判断正确的是( )
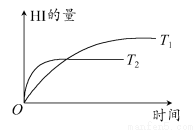
A.T1<T2,ΔH<0 B.T1>T2,ΔH<0 C.T1<T2,ΔH>0 D.T1>T2,ΔH>0
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题5微观结构与物质的多样性练习卷(解析版) 题型:选择题
短周期元素甲、乙、丙、丁、戊五种元素在元素周期表中的位置如右图所示,其中戊是同周期中原子半径最小的元素。下列有关判断正确的是( )

A.最外层电子数:甲>乙>丙>丁>戊
B.简单离子的离子半径:戊>丁
C.含有丁元素的酸有多种
D.乙的氢化物多种多样,丙、丁、戊的氢化物各有一种
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题3从矿物到基础材料练习卷(解析版) 题型:选择题
将1.12 g铁粉加入25 mL 2 mol/L的FeCl3溶液中,充分反应后,其结果是( )
A.铁有剩余,溶液呈浅绿色,Cl-浓度基本不变
B.向溶液中滴入无色的KSCN溶液,显血红色
C.Fe2+和Fe3+的物质的量之比为5:1
D.氧化产物与还原产物的物质的量之比为2:5
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题3从矿物到基础材料练习卷(解析版) 题型:选择题
硅作为一种新型能源被广泛开发利用,关于其有利因素下列说法中,你认为不正确的是( )
A.硅燃烧产物对环境产生的污染,容易得到有效控制
B.从Si(s)+O2(g)  SiO2(s) ΔH=-858.6 kJ·mol-1可知,硅燃烧放出的热量多
SiO2(s) ΔH=-858.6 kJ·mol-1可知,硅燃烧放出的热量多
C.自然界中硅的贮存量丰富,可以从自然界直接获得单质硅
D.硅便于运输、贮存,从安全角度考虑,硅是最佳的燃料之一
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题2从海水中获得的化学物质练习卷(解析版) 题型:选择题
NaCl是一种化工原料,可以制备一系列物质(如图所示)。下列说法正确的是( )
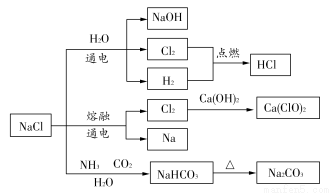
A.25℃,NaHCO3在水中的溶解度比Na2CO3的大
B.石灰乳与Cl2的反应中,Cl2既是氧化剂,又是还原剂
C.常温下干燥的Cl2能用钢瓶贮存,所以Cl2不与铁反应
D.如图所示转化反应都是氧化还原反应
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题2从海水中获得的化学物质练习卷(解析版) 题型:选择题
如图所示,四条直线分别表示钠、镁、铝、铁与足量Cl2反应时消耗金属的质量(纵轴)与反应掉的氯气质量(横轴)的关系,其中代表铁与Cl2反应的直线是( )
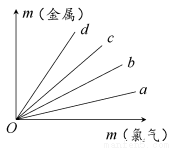
A.a B.b C.c D.d
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题1化学家眼中的物质世界练习卷(解析版) 题型:选择题
下列与化学概念有关的说法正确的是( )
A.化合反应均为氧化还原反应
B.金属氧化物均为碱性氧化物
C.催化剂能改变可逆反应达到平衡的时间
D.石油是混合物,其分馏产品汽油为纯净物
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题12物质结构与性质练习卷(解析版) 题型:选择题
下列各组原子中,彼此的化学性质一定相似的是( )
A.P原子:1s2;Q原子:2s2
B.P原子:M能层上有2个电子;Q原子:N能层上有2个电子
C.P原子:2p能级上有1个未成对电子;Q原子:3p能级上也有1个未成对电子
D.P原子:最外层L能层上只有一个空轨道;Q原子:最外层M能层上也只有一个空轨道
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com