
电解原理在化学工业中有广泛的应用。如图表示一个电解池,装有电解液c;A、B分别是两块电极板,通过导线与直流电源相连。
(1)若A、B都是惰性电极,电解质溶液c是饱和NaCl溶液,实验开始时,同时在U形管两边各滴入几滴酚酞溶液,试判断①a是________极(填“正”或“负”),B是________极(填“阴”或“阳”);
②A电极上的电极反应式为__________________,
B电极上的电极反应式为________________________;
③检验A电极产物的方法是_____________________。
(2)用惰性电极电解CuSO4溶液。若阴极上析出Cu的质量为3.2 g,则阳极上产生的气体在标准状况下的体积为________;常温下,若将电解后的溶液稀释至1 L,则溶液的pH约为________。
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:
已知:Fe2O3(s)+  C(s)====
C(s)====  CO2(g)+2Fe(s) ΔH=+234.1 kJ/mol
CO2(g)+2Fe(s) ΔH=+234.1 kJ/mol
C(s)+O2(g)====CO2(g) ΔH=-393.5 kJ/mol
则2Fe(s)+  O2(g)====Fe2O3(s)的ΔH是( )
O2(g)====Fe2O3(s)的ΔH是( )
A.-824.4 kJ/mol B.-627.6 kJ/mol C.-744.7 kJ/mol D.-169.4 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下列能说明氯元素原子得电子能力比硫强的是( )
①HCl的溶解度比H2S大 ②HCl的酸性比H2S强③HCl的稳定性比H2S强 ④HCl的还原性比H2S强⑤HClO的酸性比H2SO4强 ⑥Cl2能与H2S反应生成S ⑦Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑧还原性:Cl- <S2-
A.③④⑤⑧ B.③⑥⑦ C.③⑥⑦⑧ D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.有些物质是由原子直接构成,如金刚石、水晶等;有些物质是由分子直接构成,如干冰、氯化铵等;有些物质是由离子直接构成的,如食盐、烧碱等
B.BF3、H2O、SiCl4、PCl5四种分子中所有原子都满足最外层为8电子结构
C.非金属氧化物不都是酸性氧化物;碱性氧化物都是金属氧化物
D.硫单质的熔点比钠单质的熔点高,这是由于前者比后者有更大的范德华力所致
查看答案和解析>>
科目:高中化学 来源: 题型:
2011年3月15日,CCTV-1在3·15特别行动节目中,曝光了双汇在食品生产中使用“瘦肉精”猪肉,一时间市场哗然。“瘦肉精”又称克伦特罗,其结构简式如下图。下列有关“瘦肉精”的说法不正确的是( )
A.它的分子式为C12H18N2Cl2O
B.它含有氨基、氯原子、羟基等官能团
C.1mol克伦特罗最多能和3 molH2发生加成反应
D.一定条件下它能发生水解反应、消去反应、氧化反应、加聚反应等
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机物的说法中正确的
A.2013年11月20日山东现‘夺命快递’----化学品泄漏致1死7中毒。该化学品为氟乙酸甲酯它是无色透明液体,溶于乙醇、乙醚,不溶于水。它属于酯类,也属于卤代烃
B.按系统命名法, 的名称为2,7,7-三甲基-3-乙基辛烷
的名称为2,7,7-三甲基-3-乙基辛烷
C.甲基环己烷环上一氯代物的数目为3
D.有一种信息素的结构简式为CH3(CH2)5CH===CH(CH2)9CHO,为验证该物质中既含有醛基又含有碳碳双键,向该物质的试液中先加溴的CCl4溶液,观察到溶液褪色,继续滴加直到溶液变为红棕色,再向溶液中加入0.5 mL H2O,充分振荡,观察到溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
[化学——选修3物质结构与性质](15分)
M是原子序数<30的一种金属,常用于航空、宇航、电器及仪表等工业部门,M原子的最外层有空轨道,且有两个能级处于电子半充满状态。
(1)M原子的外围电子排布式为_____________________,在周期表中属于 区元素。
(2)M的堆积方式属于钾型,其晶胞示意图为______(填序号)。

(3)MCl3·6H2O有三种不同颜色的异构体
A、[M(H2O)6]Cl3,B、[M(H2O)5Cl]Cl2·H2O和C、[M(H2O)4Cl2]Cl·2H2O。为测定蒸发MCl3溶液析出的暗绿色晶体是哪种异构体,取0.010 mol MCl3·6H2O配成溶液,滴加足量AgNO3溶液,得到沉淀2.870 g。该异构体为_______________ (填A或B或C)。
(4) MO2Cl2常温下为暗红色液体,熔点-96.5℃,沸点117℃,能与丙酮(CH3COCH3)、CCl4、CS2等互溶。
①固态MO2Cl2属于________晶体;
②CS2中碳原子和丙酮(CH3COCH3)羰基中的碳原子分别采取的杂化方式为______杂化和________杂化。
(5)+3价M的配合物K[M(C2O4)2(H2O)2]中,配体是______,与C2O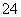 互为等电子体的分子是(填化学式)__________。
互为等电子体的分子是(填化学式)__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知滤渣2的主要成分是Fe(OH)3和Al(OH)3,由滤渣2制取Al2(SO4)3·18H2O,该探究小组设计了如下实验方案:

下列关于此方案的说法,错误的是
A.加入NaOH溶液后过滤,滤渣为Fe(OH)3
B.也可以先加硫酸,再加NaOH溶液后蒸发、冷却、结晶、过滤
C.加硫酸后,溶液中的盐除含有硫酸铝外,还有硫酸钠
D.如果滤渣2中含1molAl(OH)3,则至少需要1molNaOH才能使Al(OH)3完全溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、L、M、N六种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是短周期原子半径最大的元素,N是地壳中含量最高的金属元素。
用化学用语回答下列问题:
(1) M在元素周期表中的位置为 ;六种元素的原子半径从大到小的顺序是
(2)Z、X两元素按原子数目比l∶3构成分子A, A的电子式为
Y、L两元素按原子数目比l∶2构成分子B,B中所含的化学键类型为
(3)硒(se)是人体必需的微量元素,已知非金属性:34Se<L。请结合原子结构解释原因
(4)用Y、L、M构成的正盐溶液可以清除油污,请结合离子方程式以及必要的文字解释原因
(5)用石墨作电极,NCl3溶液作电解液进行电解,生成难溶物R,R受热分解生成化合物Q。写出电解熔融Q制取N的电极方程式:阳极: ;阴极:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com