
A、对硝基甲苯的结构简式为: |
| B、“地沟油”禁止食用,但可以用来制肥皂 |
| C、升高温度,一般可使活化分子的百分数增大,因而反应速率增大 |
| D、H2(g)+Cl2(g)═2HCl(g)△H=-184.6 kJ/mol不是氢气的燃烧热方程式 |
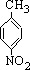 ,故A错误;
,故A错误;

科目:高中化学 来源: 题型:
| A、生成物能量一定低于反应物总能量 |
| B、相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量 |
| C、根据盖斯定律,可计算某些难以直接测定的化学反应的反应焓变 |
| D、同温同压下,H2(g)+Cl2(g)═2HCl(g)在光照和点燃条件的△H不同 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙烯使溴水、酸性高锰酸钾溶液褪色的原理相同 |
| B、乙醇可被直接氧化生成乙酸且乙醇与都能与单质钠反应 |
| C、淀粉、蔗糖、葡萄糖、蛋白质在稀硫酸中均能发生水解反应 |
| D、淀粉和聚乙烯都是天然的高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、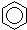 +HNO3 +HNO3
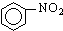 +H2O;取代反应 +H2O;取代反应 | |||
| B、CH4+Cl2→CH3Cl+HCl;置换反应 | |||
C、CH2═CH2+H2O
| |||
D、2CH3CH2OH+O2
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:钠>磷>氟>氢 |
| B、酸性:HClO4>H2SO4>H3PO4 |
| C、热稳定性:碘化氢>溴化氢>氟化氢 |
| D、还原性:S2->Cl->F- |
查看答案和解析>>
科目:高中化学 来源: 题型:
 A、T、X、Y、Z是中学化学常见的四种元素,原子序数依次增大,其结构或性质信息如下表:
A、T、X、Y、Z是中学化学常见的四种元素,原子序数依次增大,其结构或性质信息如下表:| 元素 | 结构或性质信息 |
| T | 基态原子的L层上s电子数等于p电子数 |
| X | 基态原子最外层未成对电子数在该元素所在周期中最多 |
| Y | 基态原子的第一电离能在该元素所在周期中最小 |
| Z | 单质常温、常压下是气体.基态原子的M层上有1个未成对的p电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com