
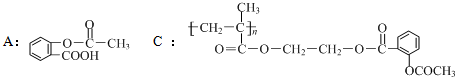
 ,B是通过加聚反应得到的,则其单体为
,B是通过加聚反应得到的,则其单体为 ;
; ;
; +H2O
+H2O| 水解 |
 +CH3COOH;
+CH3COOH; ;取样,滴入FeCl3溶液,观察到溶液呈紫色,证明已水解,反之则没有水解.
;取样,滴入FeCl3溶液,观察到溶液呈紫色,证明已水解,反之则没有水解.


科目:高中化学 来源: 题型:
| A、轮船水线以下的船壳上镶嵌有一定量的锌块 |
| B、黄铜(铜锌合金)制作的铜锣不易产生铜绿 |
| C、锌跟稀硫酸反应制取氢气,加入少量硫酸铜能加快反应速率 |
| D、铝在空气中不易腐蚀,不用特殊方法保存 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 时间t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| 总压强P l00kPa | 4 | 4.6 | 5.4 | 5.8 | 6 | 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 73 |
查看答案和解析>>
科目:高中化学 来源: 题型:
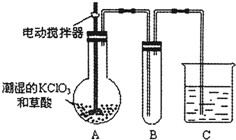
 CuCl2溶液中的铜主要以Cu(H2O)42+、CuCl42-形式存在,它们间有如下转化关系:Cu(H2O)42+(蓝色)+4Cl-?CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电.如图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝.回答下列问题:
CuCl2溶液中的铜主要以Cu(H2O)42+、CuCl42-形式存在,它们间有如下转化关系:Cu(H2O)42+(蓝色)+4Cl-?CuCl42-(黄色)+4H2O;电解不同浓度的CuCl2溶液,均可看做Cu2+、Cl-直接放电.如图为电解浓度较大CuCl2溶液的装置,实验开始后,观察到丙中的KI-淀粉溶液慢慢变蓝.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
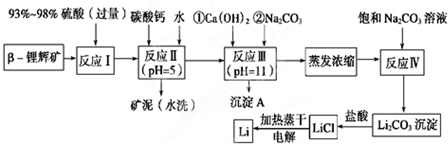
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 2.7 | 3.7 | 9.6 |
| 完全沉淀pH | 3.7 | 4.7 | 11 |
| 温度/℃ | 0 | 10 | 20 | 50 | 75 | 100 |
| Li2CO3的溶解度/g | 1.539 | 1.406 | 1.329 | 1.181 | 0.866 | 0.728 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | ① | ② | ③ | ④ |
| 溶液 | 氨水 | 氢氧化钠溶液 | 盐酸 | 醋酸溶液 |
| pH | 11 | 11 | 3 | 3 |
| A、水的电离程度:①=②=③=④ |
| B、分别加水稀释10倍,溶液的pH:①>②>③>④ |
| C、①、③两溶液等体积混合:c(Cl-)>c(NH4+)>C(H+)>c(OH-) |
| D、V1 L溶液②与V2 L溶液③混合,若V1:V2=9:11,则混合溶液pH=4(忽略溶液体积变化) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com