
【题目】下列说法正确的是( )
A.将海水中钢闸门连接电源正极可防止其被腐蚀
B.常温下,向![]() 溶液中加入少量
溶液中加入少量![]() 固体,溶液中
固体,溶液中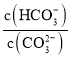 值减小
值减小
C.反应![]() 浓
浓![]() 的
的![]() ,
,![]()
D.对硫酸工业中的反应:![]() ,采用
,采用![]() 左右的高温主要是为了加快反应速率
左右的高温主要是为了加快反应速率
科目:高中化学 来源: 题型:
【题目】目前,科学界拟合成一种“双重结构”的球形分子,即把足球烯C60的分子容纳在Si60分子中,外面的硅原子与里面的碳原子以共价键结合,下列叙述错误的是( )
A.该晶体为原子晶体B.该物质的熔沸点较低
C.该物质是新化合物D.该物质的相对分子量质量为2400
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某黄色矿物中主要成分X仅含三种元素,不含结晶水,某研究小组为了探究X的组成和性质,设计并完成了如下实验:
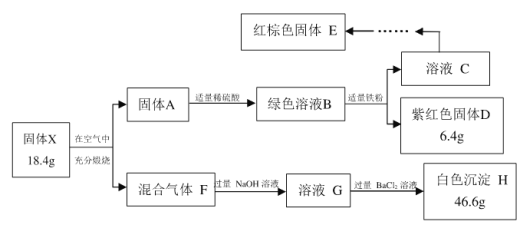
注:适量代表该试剂恰好完全反应
(1)固体X中所含元素有Fe、S和___________,其化学式为___________;
(2)F→G的总离子方程式(只写一步)是_____________________________________,该反应的还原剂是_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。
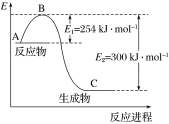
(1)上图是N2(g)和H2(g)反应生成1 mol NH3(g)过程中能量的变化示意图,请写出N2和H2反应的热化学方程式:______________。
(2)若已知下列数据:
化学键 | H—H | N≡N |
键能/kJ·mol-1 | 435 | 943 |
试根据表中及图中数据计算N—H的键能:________ kJ·mol-1。
(3)用NH3催化还原NOx还可以消除氮氧化物的污染。已知:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) ΔH1=-a kJ·mol-1①
N2(g)+O2(g)===2NO(g) ΔH2=-b kJ·mol-1②
若1 mol NH3还原NO至N2,则该反应过程中的反应热ΔH3=________ kJ·mol-1(用含a、b的式子表示)。
(4)捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
反应Ⅰ:2NH3(l)+H2O(l)+CO2(g) ![]() (NH4)2CO3(aq) ΔH1
(NH4)2CO3(aq) ΔH1
反应Ⅱ:NH3(l)+H2O(l)+CO2(g) ![]() NH4HCO3(aq) ΔH2
NH4HCO3(aq) ΔH2
反应Ⅲ:(NH4)2CO3(aq)+H2O(l)+CO2(g) ![]() 2NH4HCO3(aq) ΔH3
2NH4HCO3(aq) ΔH3
则ΔH3与ΔH1、ΔH2之间的关系是ΔH3=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是部分短周期主族元素原子半径与原子序数的关系图。下列说法正确的是( )
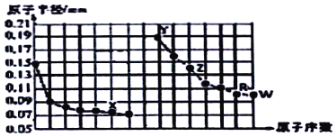
A.X所在主族中,X的简单氢化物分子间存在氢键,所以其氢化物稳定性最强
B.R简单氢化物的酸性弱于W简单氢化物,故元素非金属性R小于W
C.在同周期中,W的含氧酸酸性最强
D.Y的氢化物可以与水反应,产生一种单质气体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,相同pH的氢氧化钠和醋酸钠溶液加水稀释,平衡时pH随溶液体积变化的曲线如下图所示,则下列叙述正确的是

A.b、c两点溶液的导电能力相同
B.a、b、c三点溶液中水的电离程度a>c>b
C.c点溶液中c(H+) =c(OH-) +c(CH3COOH)
D.用等浓度的盐酸分别与等体积的b、c处溶液恰好完全反应,消耗盐酸体积 Vb = Vc
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醛(HCHO)在化工、医药、农药等方面有广泛的应用。
⑴甲醇脱氢法可制备甲醛,反应方程式为CH3OH![]() HCHO+H2。
HCHO+H2。
①发生反应时的过程如图所示,从热效应角度判断,可知该反应为______反应。

②下列方法中能减慢反应速率的是______(填字母)。
a.使用催化剂 b.升高温度 c.降低反应物浓度
③使用催化剂________(填“能”或“不能”)使反应物的转化率达到100%。
⑵甲醛超标会危害人体健康,需对甲醛含量检测及处理。
①某甲醛气体探测仪利用燃料电池工作原理,其结构如图所示。电极a为______(填“正”或“负”)极,在电极b上发生的反应类型为______反应。(填“氧化”或“还原”)

②探测仪工作时,电子从______极流出(填“a”或“b”),总反应方程式为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生产、生活息息相关。现有下列4种有机物:①乙炔 ②乙二醇 ③甲苯 ④苯酚,请将相应的序号填入空格内。
(1)用做汽车防冻剂的是___;
(2)可用于杀菌消毒、制造阿司匹林等,俗称石炭酸的是___;
(3)常用来焊接或切割金属的是___。
(4)制造烈性炸药TNT的化学方程式是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表,下列说法错误的是
物质 | X Y Z |
初始浓度/mol·L-1 | 0.1 0.2 0 |
平衡浓度/mol·L-1 | 0.05 0.05 0.1 |
A.反应达到平衡时,X的转化率为50%
B.反应可表示为X+3Y![]() 2Z
2Z
C.平衡常数 K = 1600 mol-2·L2
D.增大压强和升高温度,平衡正方向移动
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com